« zurück zur Übersicht - Projektarbeiten
"Erprobung von Verfahren zur Erkennung und Unterscheidung von Faserstoffen (Textilien)"
von Julia Seib und Helene Urich (Schuljahr 2004/05)
| 1. Einleitung und Problemstellung | zum Seitenanfang  |
Bis ins 19. Jahrhundert benutzte man ausschließlich Naturfasern, v.a. Baumwolle, zur Herstellung von Textilien. Erst im 20. Jahrhundert konnten die ersten vollsynthetischen Textilfasern vermarktet werden und die Baumwolle bekam zunehmend Konkurrenz. Heutzutage ist in einigen Fällen eine Unterscheidung der Synthesefasern von Naturfasern allein mit dem Auge sogar kaum noch möglich.
Unsere Sinne alleine reichen in diesem Fall also nicht aus. Es bedarf demnach spezieller Methoden, die es uns ermöglichen sollen die einzelnen Faserstoffe zu erkennen und auseinander zuhalten. Es sollte jedoch darauf geachtet werden, dass die angewandten Methoden möglichst einfach sind und ohne großen Aufwand durchgeführt werden können. Dies war die Aufgabe unserer Projektarbeit und es ist uns gelungen mit unkomplizierten Schnelltests (z.B. der Brennprobe) und einigen spezifischen Proben (z.B. der Ninhydrin-Reaktion) zum einen die natürlichen von den synthetischen und zum anderen die Fasern der beiden Sparten untereinander zu unterscheiden.
| 2. Geschichtliche Hintergründe | zum Seitenanfang  |
"Es gibt wildwachsende Bäume, aus deren Frucht man eine Wolle gewinnen kann, die die Schönheit und Qualität der Schafwolle weit übertrifft. Die Inder machen aus dieser Baumwolle ihre Kleider." [8] schrieb der griechische Historiker Herodot bereits 500 v.Chr.. Baumwolle wird seit Jahrtausenden zur Herstellung von Kleidung verwendet. Auch aus Schafwolle gewinnen Menschen schon seit Urzeiten tragfähige Textilien. Wann man gelernt hat die Seidenfaser zu verarbeiten, verliert sich im Dunkel der Vorzeit. Fakt ist jedoch, dass die Chinesen diese Kunst Tausende von Jahren vor der restlichen Welt geheim hielten.
Erst 1892 wird die Viskose in England erfunden. Doch noch immer bleibt der natürliche Rohstoff Cellulose die Basis der neuen Textilfaser. Im Jahre 1912 gelingt es F. Klatte Vinylchlorid zu polymerisieren: die Geburtsstunde der ersten vollsynthetischen Faser, des Polyvinylchlorids (PVC). Allerdings hat diese erste Synthesefaser heute nur noch geringe Bedeutung. Damals erkannte man jedoch noch nicht die makromolekulare Struktur der erzeugten Substanzen. Dies geschah erst Ende der 20er Jahre des 20. Jahrhunderts durch die Arbeiten von H. Staudinger. Damit brach das Zeitalter der Polymerchemie an und die Entwicklung der Kunststoff- und Textilindustrie war nicht mehr aufzuhalten. 1935 entdeckt W. H. Carothers das Nylon (PA 66) und P. Schlack 1938 das Perlon (PA 6), beides Fasern auf Polyamidbasis (PA). Im Jahre 1937 erfindet O. Bayer ein Verfahren zur Herstellung von Polyurethanen, welche durch Polyaddition von Diisocyanaten und Polyolen gewonnen werden. In England schaffen es 1941 J. R. Whinfield und J. T. Dickson den Kunststoff Polyester durch Erhitzen von Terephthalsäure und Ethylenglycol zu gewinnen. Heute bilden die Polyesterfasern die größte Synthesefaser-Gruppe. Die Polyacrylfasern werden schließlich 1942 von H. Rein erfunden. Seither ist eine Vielzahl von Chemiefasern dazugekommen und noch heute ist ein Ende der Entwicklung auf diesem Gebiet nicht abzusehen.
| Chemiefaser | Kurzzeichen | Entdeckungsjahr |
| Viskose | CV | 1892 |
| Polyvinylchlorid | PVC | 1912 |
| Polyamid (Nylon) | PA 66 | 1935 |
| Polyamid (Perlon) | PA 6 | 1938 |
| Polyurethan | PUR | 1937 |
| Polyester | PES | 1941 |
| Polyacryl(nitril) | PAN | 1942 |
Tab. 2: Übersicht über Chemiefasern und ihrem Entdeckungsjahr
Literatur Kapitel 2: [4] [8] [9] [10] [11] [17] [19] [21] [25]
| 3. Herstellung der Textilfasern | zum Seitenanfang  |
| 3-1. Einteilung der Faserstoffe | zum Seitenanfang  |
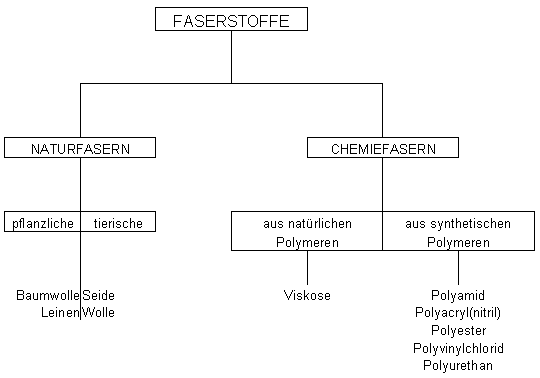
Es gibt natürlich weitaus mehr Textilfasern als oben erwähnt. Wir stellen jedoch nur diejenigen vor, die von uns zwecks unserer Projektarbeit untersucht wurden.
Literatur Kapitel 3.1: [15]
| 3-2. Herstellung der Naturfasern | zum Seitenanfang  |
Zu dieser Gruppe gehören alle Fasern natürlichen Ursprungs. Sie können von Pflanzenteilen, aus dem Fell der Tiere oder von Kokons der Seidenspinner stammen. Deshalb erfolgt die Aufteilung der Naturfasern in pflanzliche Fasern (auf Zellulosebasis), und tierische Fasern (auf Eiweißbasis).
3.2.1. Die Baumwolle (CO)
Die Baumwollpflanze:
Die Baumwolle ist das Samenhaar der Pflanze Gossypium (lat.),die zu den Malvengewächsen gehört. Ihr Anteil an Zellulose beträgt 95%. Die Anbaugebiete befinden sich in tropischen und subtropischen Zonen. Heute wird Baumwolle in Rund 80 Ländern angebaut, wobei China, USA, Russland, Indien Pakistan, Brasilien, Ägypten, Türkei und Mexiko die wichtigsten Anbauländer sind. Die Ernte erfolgt mit der Pflückmaschine oder mit den Händen. Nach der Ernte wird die Baumwolle etwa 30 Tage gelagert, damit sie trocknet und nachreift. Anschließend werden die Fasern von den Samenkörnern getrennt. Aus 100 kg Baumwolle am Kern erhält man etwa 35 kg Fasern, 62 kg Samenkörner und 3 kg Abfall.
Rohbaumwolle wird nach Faserlänge (Stapel), Gleichmäßigkeit, Feinheit, Farbe, Reinheit, Festigkeit, Reifegrad und Glanz gehandelt.
Die hochwertigsten Baumwollarten sind "Sea-Island" aus den USA (Faser kann bis 56 mm lang werden) und Mako-Baumwolle (etwa 40 mm) aus Ägypten. Eine durchschnittliche Art ist die Upland-Baumwolle (etwa 30 mm).
Baumwolle ist sehr geschätzt, weil sie preisgünstig ist, sich gut verarbeiten und veredeln lässt und viele Gebrauchseigenschaften für viele textile Einsatzbereiche besitzt.
Baumwolle wird hauptsächlich mit Polyester, Polyamid, Viskose bzw. Modalfaser gemischt. Dadurch wird die Faser strapazierfähiger und pflegeleichter. Die wichtigsten Beispiele für Baumwollfasern sind Biber, Frottier, Cord, Samt und Demin.
Zellulose, als Grundbestandteil der Baumwolle, ist ein Polysaccharid und wird aus ß-D-Glucose gebildet:
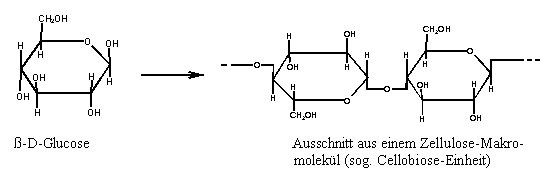
3.2.2. Leinen (Flachs) (LI)
Die Flachspflanze:
Die Flachspflanze wird wie Getreide angebaut. Die Hauptanbaugebiete sind Russland, Polen, Tschechoslowakei, Belgien, Frankreich und Irland. Die Flachsfaser wird aus dem Stengel der Pflanze gewonnen und ist daher eine Bastfaser (Stengelfaser). Die Faserbündel bestehen aus vielen Einzelfasern, die mit Pflanzenleim (= Pectin) miteinander verbunden sind.
Herstellung der Leinen:
- Raufen: die Pflanze wird mit der Wurzel aus dem boden gezogen
- Riffeln: die Stengel werden von Blättern und Samenkapseln befreit
- Rösten/Rotten: lösen der Faserbündel aus dem Stengel, indem Mikroorganismen den Pflanzenleim abbauen.
- Brechen: die Flachsstengel werden geknickt, so dass Holzteile zerkleinert werden
- Schwingen: Bastfasern werden in der Schwingmaschine von den Stengelteilen (Holzteilen) getrennt
- Hecheln: (Reinigung und Präparation für das Verspinnen) Entfernung der letzten Schäben.
Der Bast wird mit der Hechelmaschine in Faserbündel aufgeteilt, die verspinnbar sind.
Leinenfasern bestehen aus 70 % Zellulose, der Rest ist Pflanzenleim. Beide Bestandteile verleihen den Fasern Glanz, Festigkeit, Saugfähigkeit und Steifheit.
Qualitäten:
- Reinleinen:
100 % Leinen, Fester Griff und effektvolle Garnverdickungen (erkennbar, wenn Gewebe gegen das Licht gehalten wird = Lichtprobe) - Halbleinen:
Garnverdickung in nur eine Geweberichtung, der Schussrichtung; im Griff wärmer, geschmeidiger und leichter als Reinleinen; folgende Angabe ist Pflicht: "Kette reine Baumwolle - Schuss reines Leinen".
3.2.3. Die Wolle (WO)
Im Allgemeinen sind Wollfasern als Haare von verschiedenen Tieren definiert, z.B. Schaf, Kamel, Ziege, Kaninchen. Sie eignen sich zum Verspinnen und Weben. Das wichtigste Tier in der Produktion der Wolle ist das Schaf.
Die Wollfaser ähnelt dem menschlichen Haar und hat eine schuppige Oberfläche. Die Grundsubstanz ist Keratin (Eiweißmolekülketten). Am Aufbau des Keratins sind 24 verschiedene Aminosäuren beteiligt, darunter auch das schwefelhaltige Cystin.
Die Aminosäuren werden durch Peptidbindungen (Amidbindungen) verknüpft:
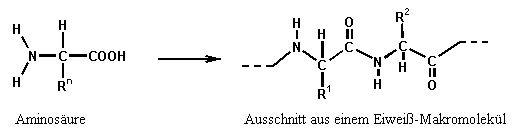
Die Hauptherkunftsländer der Wolle sind Australien, Neuseeland, Südafrika, Uruguay, China, Russland, Türkei und Argentinien. Die Wolle wird von den Körpern der Schafe abgeschoren.
Nach dem Scheren wird die Wolle gewaschen, wobei als Nebenprodukt Wollfett (Lanolin) entfernt wird, das als Basismaterial für Salben- und Hautcremeherstellung genutzt wird. Wolle wird nach ihrer Feinheit, Länge, Kräuselung, Reinheit und Herkunft beurteilet.
Die Schafrassen:
- Merinoschaf: Merino-Wolle ist fein, kurzfaserig (bis zu 100 mm) und stark gekräuselt
- Crossbredschaf: Crossbredwolle ist mittellang (bis zu 200 mm), mittlere Feinheit und verfügt über eine mittlere Kräuselung
- Cheviotschaf: Cheviot-Wolle ist lang (bis zu 500 mm), grob, wenig gekräuselt
Schurwolle:
Wolle vom lebenden, gesunden Schaf, die vorher nicht schon mal in einem Fertigprodukt verwendet wurde.
"Reine Wolle" oder "100 % Wolle" kann sich aus Regenerierter Wolle (Reißwolle) und Wolle von toten Schafen (Sterblingswolle) zusammensetzen.
3.2.4. Die Seide (SE)
Die Maulbeerseide (auch Zuchtseide genannt) wird von den Raupen des Maulbeerspinners gewonnen. Die Maulbeerspinner werden gezüchtet und ernähren sich von den Blättern der Maulbäume. Die Seidenproduzierende Länder sind China, Japan, Korea, Indien, Griechenland, Frankreich und Spanien. Die Raupen produzieren den Seidenfaden indem sie aus vier Drüsen am Unterkiefer Fibroin (Material des Seidenfadens) und Sericin (Seidenbast/Seidenleim) produzieren, dass sie für den Bau des Kokons brauchen. Nachdem die Kokons eingesammelt und die Raupen abgetötet wurden wird die Seide als eine Endlosfaser (Haspelseide) abgewickelt. Entbastete Seide bekommt man, wenn man das Sericin (Seidenbast) durch Abkochen im Seifenbad entfernt. Wegen dem entstandenen Gewichtsverlust wird die Seide mit Metallsalzen erschwert. Als die wichtigsten Seidenarten gelten die Maulbeerseide (Zuchtseide) und die Tussahseide (Wildseide).
Die Seide ist wie die Wolle eine Eiweißfaser, nur ist beim Aufbau des Fibroins die Aminosäure Cystin nicht beteiligt.
Literatur: [2] [12] [18]
| 3-3. Herstellung der Chemiefasern | zum Seitenanfang  |
Als Chemiefasern bezeichnet man Fasern, die durch Verarbeitung von natürlichen (z.B. Viskose) oder synthetischen (z.B. Polyamide) makromolekularen Verbindungen erhalten werden. Bevor man jedoch die hochmolekularen Verbindungen verarbeiten kann müssen diese zunächst hergestellt werden. Dazu benötigt man mindestens bifunktionelle Monomere, die aus Erdölprodukten gewonnen werden. Die Monomere ("Bausteinmoleküle") können dann durch verschiedene Verknüpfungsreaktionen (Polymerisation, Polykondensation oder Polyaddition) zu polymeren Molekülen zusammengesetzt werden. Erst jetzt folgt die Verarbeitung zu den gewünschten Fasern.
3.3.1. Herstellung der Viskose (CV)
Viskose wird durch die Verarbeitung von Zellulose gewonnen. Zellulose ist die Grundsubstanz in Pflanzen, die ihnen Halt und Biegsamkeit verleiht. Man kann sie als kleine Fäserchen in Pflanzen erkennen, aber sie sind im Gegensatz zu Baumwolle viel zu kurz um weiterverarbeitet zu werden. Früher wurden die kurzfaserigen Samenhaare der Baumwolle, die Linters, als Ausgangsmaterial verwendet. Heute benutzt man hauptsächlich das Holz von Laub- und Nadelbäumen. Der Gehalt von Zellulose beträgt darin 70 %. Man kocht das Holz unter hohem Druck, wobei sich alles löst außer Zellulose. Es entsteht ein Faserbrei, der als Zellulose mit hohem Reinheitsgrad (Zellstoff) in der Chemiefaserindustrie verwendet wird.
- Es werden Zellstoffblätter mit Natronlauge versetzt (Zellulose quillt - es bildet sich Alkalizellulose)
- Vorreife: es wird die durchschnittliche Länge der Kettenmoleküle so eingestellt, dass die entstehende Spinnlösung die richtige Zähflüssigkeit hat
- Sulfidierung: Alkalizellulose reagiert mit Schwefelkohlenstoff (weiße Masse wird rotgelb verfärbt - Bildung von Zellulosexanthogenat. Um sie verspinnbar zu machen wird sie durch Natronlauge gelöst.
- Spinnen mit Hilfe von Spinndüsen: Verfestigung zu Viskosefilamenten. Nassspinnverfahren: erwärmtes Fällbad neutralisiert die vorher verwendeten Chemikalien - Erstarren der Filamente; Zellulose verändert sich nicht sondern liegt dann in Faserform vor.
Das Zellulosexanthogenat enthält, wie der Name schon sagt, Xanthogenat-Reste:

So ein Rest ersetzt pro Cellobiose-Einheit ein H-Atom an einer OH-Gruppe. Bei der Faserherstellung werden diese allerdings größtenteils abgespalten, sodass Viskosefasern praktisch aus reiner Zellulose bestehen.
3.3.2. Herstellung von Polyamiden (PA)
Polyamide sind Polymere, deren einzelne Molekülglieder durch Amidbindungen miteinander verbunden sind.
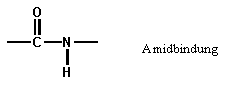
Polyamide werden durch Polykondensation von entweder einer Aminocarbonsäure oder von einer Dicarbonsäure und einem Diamin gewonnen. Um die zwei unterschiedlichen Arten von Polyamiden unterscheiden zu können gibt es, außer dem systematischen Namen, noch nach der DIN vereinbarten Kurzzeichen. Dieser Sachverhalt wird im Folgenden an zwei bekannten Beispielen erläutert.
-
Perlon
Perlon ist das Polykondensat von epsilon-Caprolactam bzw. der daraus gewonnenen epsilon-Aminocapronsäure:
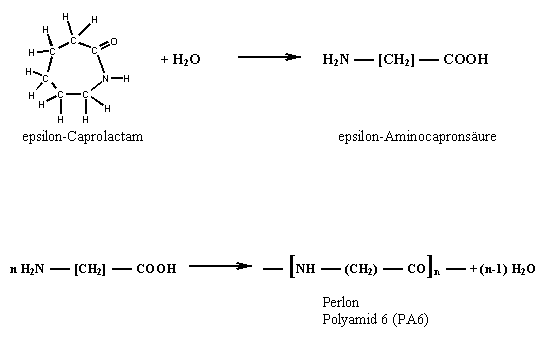
Polyamide mit einer Aminocarbonsäure als Monomeres werden mit den Buchstaben PA, für Polyamid, und einer nachgestellten arabischen Zahl gekennzeichnet (hier 6). Diese Zahl teilt uns mit, aus wie vielen Kohlenstoffatomen die verwendete Aminocarbonsäure besteht.
-
Nylon:
Nylon entsteht durch Polykondensation von Hexamethylendiamin (1,6-Hexandiamin) und Adipinsäure (Hexandisäure):
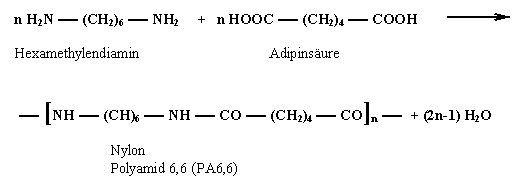
Polyamide, die durch Verknüpfung zweier verschiedener Monomere gebildet werden, werden ebenfalls mit PA, aber mit zwei nachfolgenden arabischen Zahlen gekennzeichnet. Dabei gibt die erste Zahl die Anzahl der Kohlenstoffatome im Diamin-Monomeren an, während die zweite die Anzahl der Kohlenstoffatome im Dicarbonsäure-Baustein wiedergibt.
Nylon- und Perlonfasern werden vor allem in Damenstrümpfen und Sportbekleidung verarbeitet. Nylonfasern werden auch zur Herstellung von Fallschirmen, Fischereinetzen, Angelschnüren und Ähnliches verwendet.
vspace="5"
3.3.3. Herstellung von Polyacrylnitril (PAN)
In einer Polymerisationsreaktion reagieren Acrylnitril-Moleküle zu Polyacrylnitril (PAN), welches dann zu Textilfasern weiter verarbeitet werden kann.
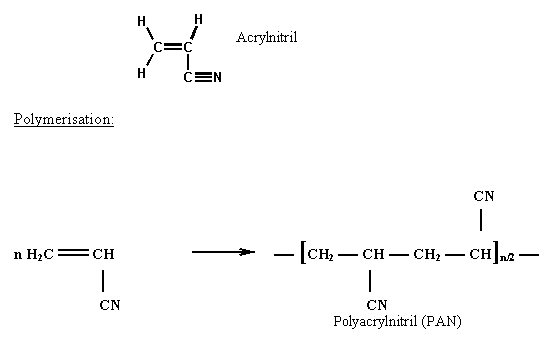
In der Textilindustrie wird Polyacrylnitril jedoch nie rein, sondern als Bestandteil von Copolymeren eingesetzt. Bei einem Acrylnitril-Anteil von 85% wird die Faser als Polyacryl und bei einem Anteil von 35-38% als Modacryl (MAC) bezeichnet. Im ersten Fall wird üblicherweise Polymethylmethacrylat (PMMA) (siehe Anhang Seite 42) und im zweiten Polyvinylchlorid (PVC) als Copolymer eingesetzt. Übliche Handelsnamen für die wollähnliche Faser sind Dralon, Orlon und Dolan.
3.3.4. Herstellung von Polyester (PES/PET)
Polyester ist eine Sammelbezeichnung für Polymere, deren Grundbausteine durch Esterbindungen zusammengehalten werden.
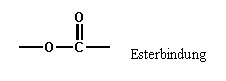
Der bekannteste und wichtigste Vertreter dieser Stoffklasse ist heute das Polyethylenterephthalat, welches durch Polykondensation von Terephthalsäure (p-Benzoldicarbonsäure) und Glykol (Ethandiol) entsteht:
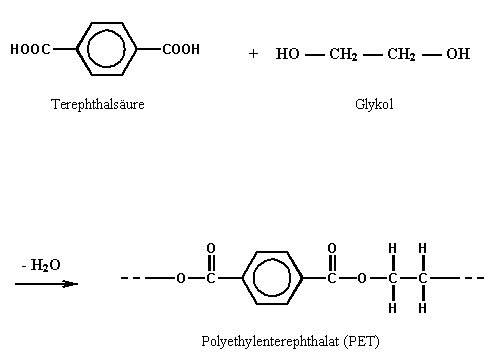
PET ist ein Vertreter der Polyester vom Typ II, da es aus zwei verschiedenen Monomeren hergestellt wird, aus einer Dicarbonsäure und einem Diol. Zu Typ I dagegen gehören solche, die durch Polykondensation von Hydroxydicarbonsäuren gewonnen werden. Heute bilden die Polyesterfasern die mit Abstand größte Synthesefaser-Gruppe.
3.3.5. Herstellung von Polyurethan (PUR)
Im Allgemeinen werden Polyurethane, durch Polyaddition aus zwei- oder höherwertigen Alkoholen und Isocyanaten erhalten. Nur die linearen eignen sich dabei zur Herstellung der sog. Elastanfasern (PUE). Elastan ist ein Elastomer, das zu mindestens 85% aus Polyurethan besteht. In großem Umfang verwendet man auch Polyurethan (PUR) als Mikroschaum für atmungsaktive Membrane bei Regen- und Winterbekleidung.
Polyurethane enthalten Polyurethanbindungen:
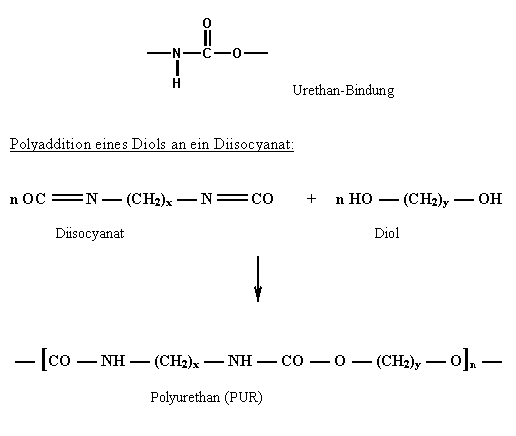
3.3.6. Herstellung von Polyvinylchlorid (PVC)
Polyvinylchlorid ist das Polymerisationsprodukt von Vinylchlorid (Chlorethen).
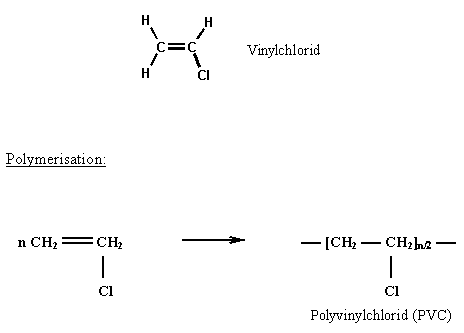
Als Material für Fasern hat PVC nur einen beschränkten Anwendungsbereich, nämlich für schwer entflammbare Gewebe, Säureschutzkleider, Regenkleidung und Ähnliches. Technische Bedeutung für die Faserherstellung haben Copolymere des Vinylchlorids z.B. mit Acrylnitril.
3.3.7. Der Spinnprozess
Das Schmelzspinnverfahren
Das zu bearbeitende Material wird geschmolzen und durch eine beheizte Spinndüse gepresst. Durch intensive anschließende Luftkühlung erstarren die Fibrillen und werden auf einer Spinnrolle gesammelt.Das Trockenspinnverfahren
Die Polymermasse wird gelöst und anschließend in einen beheizten Schacht gepresst. Das Lösungsmittel verdampft in der warmen Luft und die Faser wird hart. Schließlich verstreckt man die Faser und wickelt sie auf.Das Nassspinnverfahren
Dieses Verfahren wird bei allen Fasern aus abgewandelten Naturstoffen eingesetzt (z.B. bei Viskose). Die zu verarbeitende Masse wird dabei in ein Fällbad gesponnen, die ausgefällte Faser gewaschen, getrocknet und aufgerollt.
Literatur Kapitel 3: [2] [3] [5] [9] [12] [14] [15] [18] [19] [20] [21] [25]
| 4. Die Faseridentifizierung | zum Seitenanfang  |
| 4-1. Einführung | zum Seitenanfang  |
Zu Beginn sei erwähnt, dass alle Untersuchungsmethoden, deren Durchführung und Auswertung in diesem Kapitel beschrieben werden, nur bei Einzelfasern angewendet werden können. Um Mischfasern auf dieselbe Art und Weise untersuchen zu können, müssten diese in die einzelnen Komponenten zerlegt werden, was mit einem großen Zeitaufwand verbunden wäre.
Folgende Prüfmethoden dienten in unserer Projektarbeit zur Identifizierung der in Kapitel 3 genannten Fasern:
- Schnellmethoden
- Brennprobe
- Trockene Destillation
- Verhalten in ausgewählten Lösungsmitteln (Säuren, Laugen, organische Lösemitteln)
- Spezifische Tests
- Ninhydrin-Reaktion (für Wolle und Seide)
- Biuret-Reaktion (für Wolle und Seide)
- Plumbad-Reaktion (für Wolle)
- Beilstein-Probe (für PVC)
Die Durchführung der genannten Versuche erfolgt immer im Abzug. Außerdem ist stets auf angemessene Schutzkleidung (Schutzbrille und Schutzmantel)zu achten.
| 4-2. Die Brennprobe | zum Seitenanfang  |
Materialien:
- Bunsenbrenner
- Keramikplatte als feuerfeste Unterlage
- Tiegelzange
- Feuerzeug
Durchführung:
Ein kleines Stück des Faserstoffs wird mit der Tiegelzange für kurze Zeit in die Randzone der Brennerflamme gehalten. Es wird darauf geachtet, wie schnell sich die Faser entzündet und ob sie außerhalb der Flamme weiterbrennt oder eher zum Erlöschen neigt. Weiter betrachtet man das Verhalten der Faser in der Flamme. Wichtig dabei ist, ob die Faser schmilzt oder nicht. Auch wird auf eventuelle Rußbildung, den entstandenen Geruch und auf die Art des Rückstandes Acht gegeben. Die feuerfeste Unterlage hält man stets unter die Faser, falls Bruchstücke oder Schmelze herabfallen.
Beobachtungen:
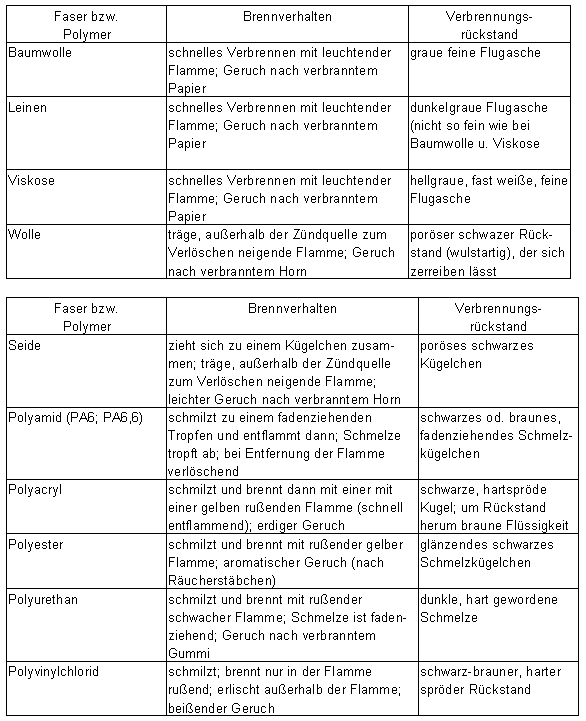
Tab. 4.2: Brand- und Entzündungsverhalten der Textilfasern
Auswertung:
Das Brennverhalten von Faserstoffen hängt von der Zusammensetzung des jeweiligen Polymers ab.
Eine Verbrennung läuft in Form von Kettenreaktionen ab. Als Kettenüberträger wirken vor allem *OH- und *H-Radikale.
Beispiel einer solchen Kettenreaktion:
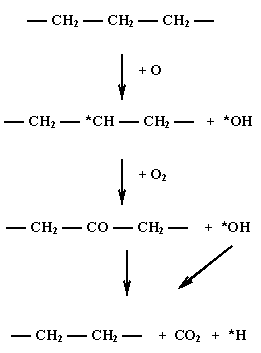
Halogenhaltige Polymere spalten in der Hitze Halogenwasserstoffe ab, was bedeutet, dass PVC Chlorwasserstoff abspaltet, der besonders die reaktiven *OH- und *H-Radikale in weniger kritische Moleküle umwandelt. Die dabei entstehenden Chlorradikale (*Cl) "entschärfen" noch aktive Sauerstoffatome (O).:
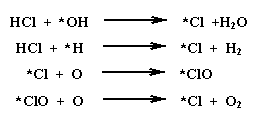
Weniger effektive Wirkungen haben stickstoffhaltige und ferner schwefelhaltige Verbindungen.
Die Zellulosefasern enthalten keines dieser Elemente. Aus diesem Grund sind sie sehr leicht entzündlich und verbrennen schnell. Auch Polyesterfasern gehören nicht zu den schwerentflammbaren Textilien. Stickstoffatome sind Bestandteil von Polyamid-, Polyacryl- und Polyurethanpolymeren, die deswegen nicht so unbeschwert verbrennen wie z.B. Baumwolle. Proteinfasern sind ebenfalls stickstoffhaltig, wobei bei der Wolle noch zusätzlich Schwefelatome hinzukommen. Diese Tatsache ist für die relativ schwere Entzündbarkeit der Seide und Wolle verantwortlich.
Literatur Kapitel 4.2: [3] [6] [7] [14] [15] [24]
| 4-3. Die trockene Destillation | zum Seitenanfang  |
Materialien:
- Bunsenbrenner mit Keramikplatte
- Reagenzgläser, Reagenzglasständer, Reagenzglasklammer
- pH-Indikatorpapier
- Feuerzeug
- Filterpapier
- Bleiacetat-Trihydrat (Pb(CH3COO)2 • 3H2O, reinst)
- Laborwaage
- demineralisiertes Wasser
Herstellen der 1%igen Bleiacetatlösung:
Es werden 1g Bleiacetat (Pb(CH3COO)2 • 3H2O, reinst) in ein Becherglas eingewogen und mit etwas demineralisiertem Wasser versetzt, sodass sich die Substanz vollständig löst. Danach wird bis zur 100mL-Marke aufgefüllt.
Durchführung:
Es wird eine Probe des zu untersuchenden Faserstoffs vorsichtig in einem trockenen Reagenzglas erhitzt. Man feuchtet nun ein Stück Indikatorpapier an und hält es in das Reagenzglas. Je nach Faser färbt es sich rot oder blau. Es wird dann die Farbe mit der Farbskala auf der pH-Papierschachtel verglichen und der zugehörige pH-Wert abgelesen. Nun prüft man den Geruch, indem man sich den Dampf vorsichtig mit der Hand zufächelt.
Beobachtungen:
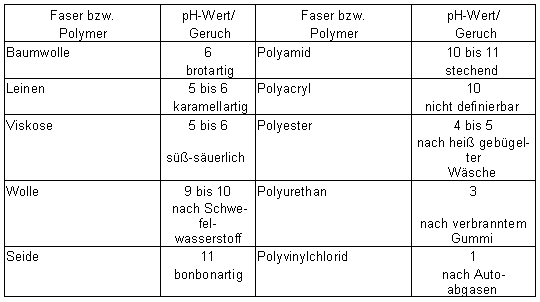
Tab.4.3.1: pH-Werte der Dämpfe bei der Trockenen Destillation
Ergänzung:
Bei Wolle ist der Geruch nach Schwefelwasserstoff auffallend. Um diesen sicher nachweisen zu können wird ein Filterpapier in die 1%ige Bleiacetatlösung getaucht und in den entstandenen Dampf gehalten.
Nur bei Wolle färbt sich das Filterpapier dunkel-braun bis schwarz, da Bleisulfid gebildet wurde.(Zugehörige Reaktionsgleichung siehe Seite).
Auswertung:
Bei der trockenen Destillation werden die Fasern durch die Wärmezufuhr thermisch zersetzt. Es finden Abbaureaktionen statt, bei denen verschiedene Substituenten abgespalten werden. Flüchtige Zersetzungsprodukte entweichen und es kann mit feuchtem Indikatorpapier auf saure, basische oder neutrale Wirkung dieser geprüft werden. Mögliche Abbauprodukte werden in Tabelle 4.3.2 aufgeführt. Die optisch hervorgehobenen sind für den pH-Wert der Dämpfe verantwortlich.
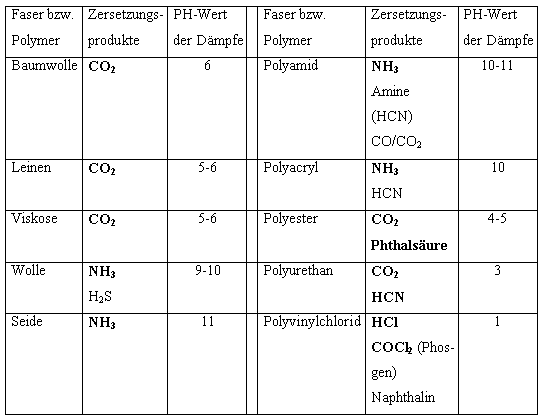
Tab.4.3.2: Abbauprodukte und deren Einfluss auf den pH-Wert
Literatur Kapitel 4.3 : [1] [3] [10] [13] [16] [24]
| 4-4. Verhalten in verschiedenen Lösungsmitteln | zum Seitenanfang  |
Materialien:
- 150 mL Bechergläser
- Bunsenbrenner mit Keramikplatte, Dreifuß und Drahtnetz
- Siedestäbe
- Laborwaage
- Demineralisiertes Wasser
- Feuerzeug
- Säuren:
- konz. Schwefelsäure (96%, reinst)
- konz. Salpetersäure (65%, reinst)
- konz. Salzsäure (10 M, reinst)
- Ameisensäure (98-100%, reinst)
- Eisessig (reinst)
- Basen:
- 40%ige Natronlauge (hergestellt aus Natriumhydroxid)
- 5%ige Natronlauge (hergestellt aus Natriumhydroxid)
- Organische Lösungsmittel:
- Aceton
- Cyclohexanon
Vorsichtsmaßnahmen:
Beim Erwärmen ist darauf zu achten, das stets ein Siedestab verwendet wird um einen Siedeverzug zu vermeiden, und dass die Lösungen nicht einkochen. Große Vorsicht bei organischen Lösungsmitteln - kein offenes Feuer! Konzentrierte Säuren und Laugen möglichst nicht einatmen. Aufpassen, dass sie nicht auf die Haut kommen (ätzend!). Alle Lösungsmittel werden fachgerecht entsorgt!
Herstellen der Laugen:
Für die 40%ige Natronlauge werden 40g und für die 5%ige 5g Natriumhydroxid (NaOH) 50mL demineralisiertes Wasser gegeben und vollständig aufgelöst. Anschließend wird bis zur 100mL-Messmarke aufgefüllt.
Durchführung:
Man legt ein Stück des zu untersuchenden Faserstoffes in ein Becherglas und versetzt es mit ca. 25 mL des Lösungsmittels. Nun wird das Verhalten der Faser etwa 10 Minuten in der kalten Lösung beobachtet. Danach wird das Ganze erwärmt (Siedestab!) und weiterhin ca. 5-10 Minuten auf das Verhalten geachtet. Man sollte darauf achten, ob sich die Faser ganz oder nur zum Teil auflöst, ob ein Zerfall der Faser oder mögliche Farbänderungen auftreten.
Beobachtungen:
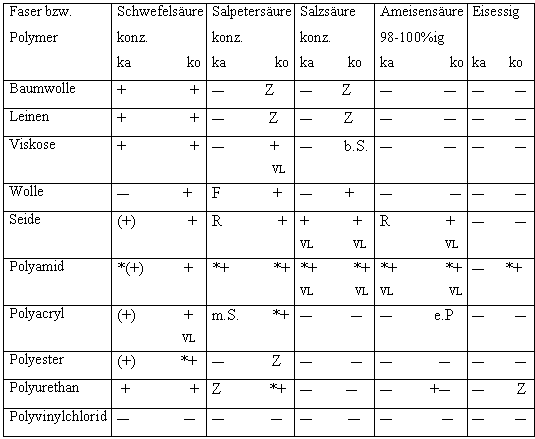
Tab.4.4.1: Verhalten der Fasern in Säuren
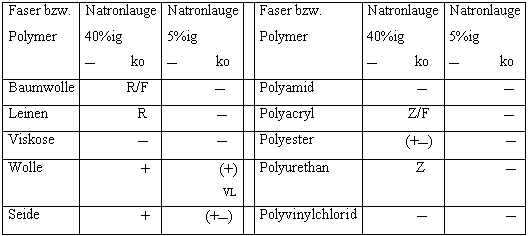
Tab.4.4.2: Verhalten der Fasern in Laugen
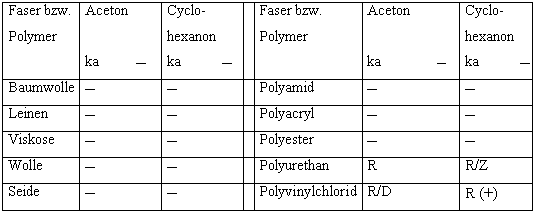
Tab.4.4.3: Verhalten der Fasern in organischen Lösungsmitteln
| Abkürzungen und Zeichenerklärungen: | |
| ka | kalt |
| ko | kochend |
| + | vollständiges Lösen nach mindestens 10 Minuten |
| __ | keine auffallende Veränderung bzw. keine Lösung |
| ( ) | Vorgang läuft langsam ab |
| +__ | nur teilweise Lösung nach mindestens 10 Minuten |
| * | beim Verdünnen tritt Ausfällung ein |
| Z | Zerfall in Bruchstücke |
| R | Zusammenrollen der Faser |
| D | Ausdehnung der Faser |
| F | Farbtonänderung der Faser: nach gelb bei Wolle und Baumwolle nach orange bei Polyacryl |
| b.S. | braune Suspension |
| m.S. | milchig-trübe Suspension |
| e.P. | "erstarrtes" Stück Plastik entsteht aus Polyacryl (Polyacryl wird hart) |
| VL | Verfärbung der Lösung: bei Wolle gelblich bei Seide rötlich bei Polyamid violett bei Polyacryl schwarz-braun bei Viskose bräunlich-orange im heißen und gelb im kalten Zustand |
Entsorgung der Lösungsmittel:
Alle Basen und Säuren werden, bevor sie in den Abfluss geleert werden, stark verdünnt. Die Ameisensäure wird mit Wasserstoffperoxid (30%) verkocht, anschließend verdünnt und in den Abfluss geleert. Alle organischen Lösungsmittel werden in den dafür vorgesehenen Behältern gesammelt.
Literatur Kapitel 4.4: [3 ]
| 4-5. Die Ninhydrin-Reaktion | zum Seitenanfang  |
Materialien:
- Ninhydrin-Sprühlösung (für der Dünnschichtchromatographie, von Merck)
- Sprühfläschchen
- Sprühkammer
- Tesafilm
- ein weißes Blatt Papier
- Fön
Vorsichtsmaßnahmen:
Hautkontakt mit dem Ninhydrin-Sprühreagenz ist zu vermeiden, da dieses die Haut violett färbt.
Durchführung:
Die zu untersuchenden Faserstoffe werden an einem Ende mit Tesafilm auf ein weißes Blatt Papier geklebt und mit zugehörigen Faserbezeichnungen beschriftet. Dieses Blatt legt man nun in die Sprühkammer (Abzug!), befüllt das Sprühfläschchen mit ausreichender Menge an Ninhydrinlösung und besprüht die Proben mit dieser. Anschließend erfolgt die Trocknung mit dem Fön.
Beobachtungen:
Nur die Seide und die Wolle verfärben sich violett. Die anderen Fasern bleiben unverändert.
Auswertung:
Das Ninhydrin-Reagenz reagiert mit den Aminosäuren der Eiweißfasern und bildet dann einen blauvioletten Farbstoff, der Ruhemann's Purpur genannt wird.
Gleichgewichtsreaktion des Ninhydrins:
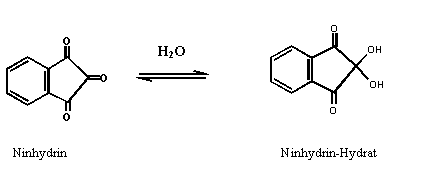
Reaktionsmechanismus:
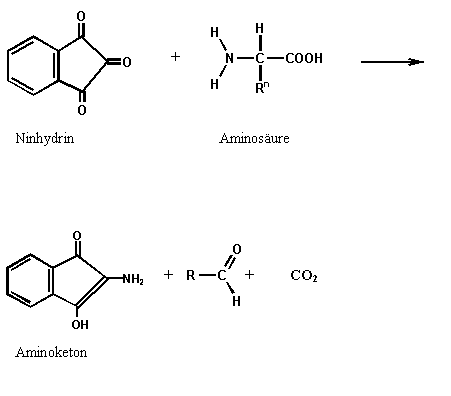
Das entstandene Aminoketon reagiert in einem zweiten Reaktionsschritt mit einem weiteren Molekül Ninhydrin. Um diesen Schritt zu beschleunigen, sollte die Temperatur erhöht werden.
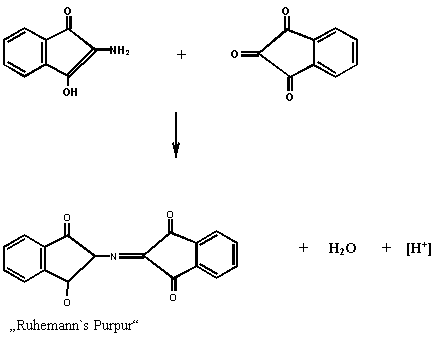
Literatur Kapitel 4.5: [21] [26]
| 4-6. Die Biuret-Reaktion | zum Seitenanfang  |
Materialien:
- Bunsenbrenner mit Keramikplatte
- Reagenzgläser, Reagenzglasständer, Reagenzglasklammer
- Siedestäbe
- Feuerzeug
- 10mL Messpipette
- 150 mL Bechergläser
- Laborwaage
- wasserfreies Kupfer(II)sulfat (CuSO4) (zur Analyse)
- Natriumhydroxid (NaOH) (technisch)
- demineralisiertes Wasser
Herstellen der benötigten Lösungen:
3%ige Kupfer(II)sulfatlösung:
Es werden 3g wasserfreies Kupfer(II)sulfat in ein Becherglas abgewogen und mit etwas demineralisiertem Wasser versetzt. Sobald sich alles gelöst hat wird bis zur 100mL-Marke aufgefüllt.
40%ige Natronlauge:
Es werden 40g Natriumhydroxid abgewogen und in ein mit 50mL befülltes Becherglas gegeben. Sobald sich alles aufgelöst hat, wird bis zur 100mL-Marke aufgefüllt.
Durchführung:
Untersuchte Fasern: Wolle und Seide
Wolle und Seide werden jeweils in 25mL der 40%igen Natronlauge im Becherglas aufgelöst. Anschließend gibt man 2-3mL der Lösungen in Reagenzgläser und versetzt sie mit 2-3 Tropfen Kupfer(II)-sulfatlösung. Als Blindprobe nimmt man demineralisiertes Wasser und versetzt dieses mit 1-2 Tropfen der Natronlauge und 2-3 Tropfen Kupfer(II)-sulfatlösung.
Beobachtungen:
Im Reagenzglas mit Wasser bildet sich ein hellblauer Niederschlag (Kupferhydroxid), während bei Wolle und Seide nichts ausfällt.
Vor Kupfer(II)-sulfatzugabe ist die Lösung der Wolle gelb und die der Seide rot. Nach der Zugabe verfärbt sich die erstere grün und die letztere dunkel-blau.
Auswertung:
Die Reaktion beruht darauf, dass die Kettenmoleküle der Proteine an ihren Stickstoffatomen mit Kupfer(II)-Ionen farbige Komplexsalze bilden:
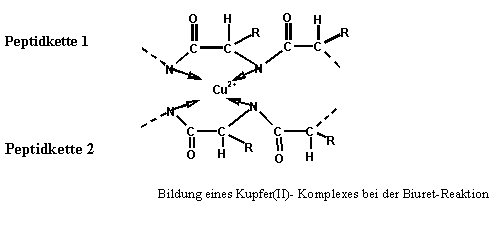
Aus diesem Grund kann im alkalischen Medium kein Kupfer(II)hydroxid ausfallen (vgl. Probe ohne gelösten Eiweiß).
Literatur Kapitel 4.6: [23]
| 4-7. Die Plumbad-Reaktion | zum Seitenanfang  |
Materialien:
- Bunsenbrenner mit Keramikpatte
- Feuerzeug
- Siedestab
- 10 mL Messpipette
- 150 mL Becherglas
- Laborwaage
- Bleiacetat-Trihydrat (Pb(CH3COO)2 • 3 H2O, reinst )
- demineralisiertes Wasser
- 3 mL Ethanol
Herstellen der Lösung:
Herstellung der 1%igen Bleiacetatlösung siehe Seite
Durchführung:
Untersuchte Faser: Wolle
Die Wolle wird mit 25mL der 1%igen Bleiacetatlösung und 3mL Ethanol versetzt. Anschließend wird die Lösung auf 80-90°C erwärmt (Siedestab!). Nun wird auf Farbveränderungen der Wolle geachtet.
Beobachtung:
Nach einigen Minuten färbt sich die Wolle schwarz.
Auswertung:
Das Eiweiß der Wolle enthält die schwefelhaltige Aminosäure Cystin. Durch die Wärmezufuhr wird diese zersetzt und es entweicht das Gas Schwefelwasserstoff (H2S), welches mit Blei(II)-Ionen das schwarze, schwerlösliche Bleisulfid bildet. Dieses ist verantwortlich für die Schwarzfärbung der Wolle.
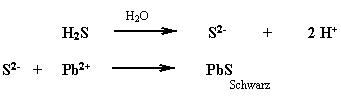
Literatur Kapitel 4.7: [21]
| 4-8. Die Beilsteinprobe | zum Seitenanfang  |
Materialien:
- Kupferblech
- Bunsenbrenner mit Keramikplatte
- Feuerzeug
- Tiegelzange
Vorsichtsmaßnahmen:
Bei der Reaktion entstehen giftige Dioxine, deshalb verwendet man ganz wenig Faserstoff.
Durchführung:
Ein Stück Kupferblech wird einige Minuten in der Brennerflamme ausgeglüht, bis eine eventuelle Blaufärbung der Flamme verschwunden ist. Anschließend wird mit der Tiegelzange ein kleines Stück des Faserstoffs auf das ausgeglühte Kupferblech gelegt und dieses dann erneut in die Flamme gehalten.
Beobachtung:
Nur mit Polyvinylchlorid kommt zu einer grünen Flammenfärbung.
Auswertung:
Polyvinylchlorid enthält Chloratome, die mit dem heißen Kupferdraht reagieren und das flüchtige Kupfer(II)-chlorid (CuCl2) bilden, welches die Flamme grün färbt.
LiteraturKapitel4.8:[23]
| 4-9. Vorgehensweise bei der Faseridentifizierung | zum Seitenanfang  |
4.9.1. Vorgehensweise bei farblosen Textilfasern
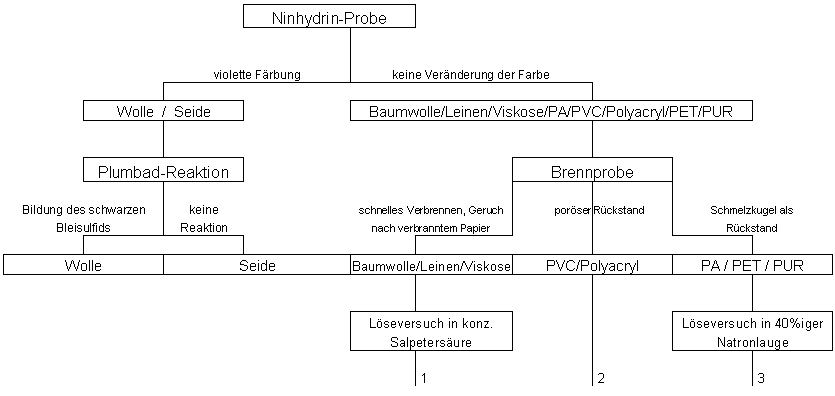
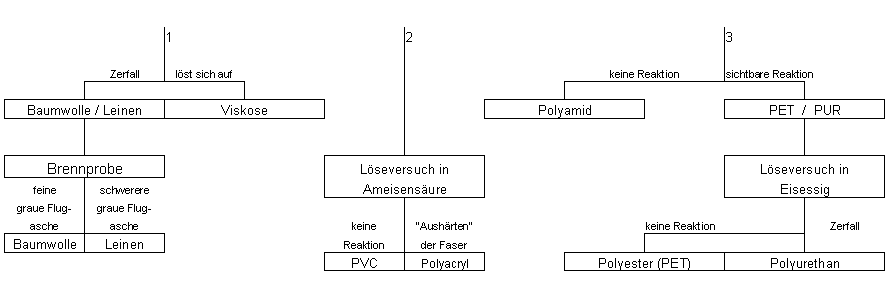
4.9.2. Vorgehensweise bei farbigen Textilfasern
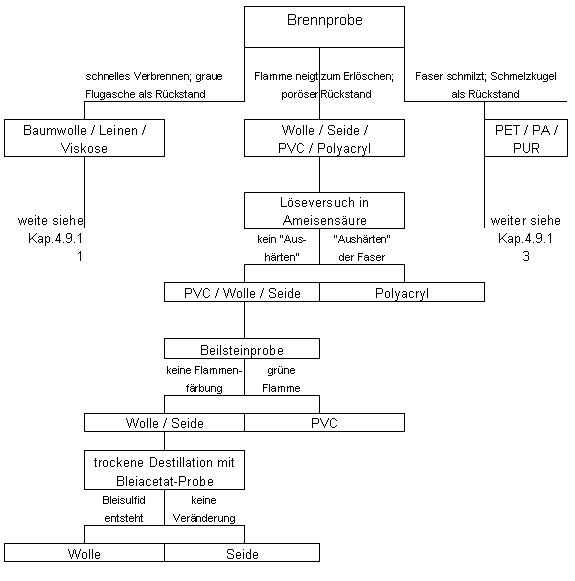
| 5. Mischfaseruntersuchung | zum Seitenanfang  |
Im Allgemeinen können Mischfasern mit den oben aufgeführten Verfahren nicht untersucht werden. Trotzdem haben wir uns dazu entschieden, die beschriebenen Methoden an einem interessanten Beispiel auszuprobieren.
Laut Etikett bestand diese Mischfaser zu 70% aus Polyacryl und zu 30% aus Wolle, also eine Mischung aus einer Natur- und einer Synthesefaser.
-
Vergleich des Verhaltens in der Flamme:

Tab.5.1: Verhalten der Mischfaser in der Flamme
Wie bereits vermutet liefert uns diese Probe keinen entscheidenden Hinweis auf die Zusammensetzung der Faser. In ihrem Verhalten in und außerhalb der Zündquelle ähnelt sie eher der Wolle als dem Polyacryl.
-
Trockene Destillation mit Prüfung der Dämpfe auf Schwefelwasserstoff:
Die Prüfung erfolgt mittels einer Geruchsprobe und einem mit Bleiacetatlösung angefeuchteten Filterpapier.

Tab.5.2: Trockene Destillation und Untersuchung der entstandenen Dämpfe
Es lässt sich also nur die Wolle eindeutig identifizieren.
-
Vergleich des Verhaltens in der Ameisensäure (98-100%ig)
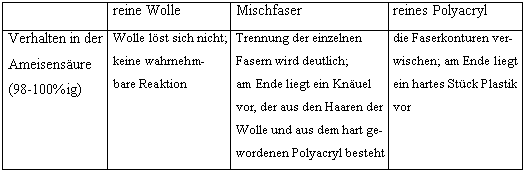
Tab.5.3: Verhalten der Fasern in 98-100%iger Ameisensäure
Wie man sieht, kann das unterschiedliche Verhalten der Fasern gegenüber einem bestimmten Medium ausgenutzt werden, um diese von einander zu trennen. In diesem Fall war die Auswahl des geeigneten Mediums, angesichts der Tatsache, dass die Zusammensetzung der Mischfaser bekannt war, selbstverständlich nicht schwer. Kennt man die einzelnen Komponenten jedoch nicht, so erweisen sich diese Methoden als nicht geeignet. Das "Aushärten" in der Ameisensäure ist in jedem Fall typisch für Polyacryl. Würde die Mischfaser aber eine dritte, in Ameisensäure lösliche Komponente enthalten, so wären wir an dieser Stelle noch lange nicht am Ende unserer Versuchsreihe.
| 6. Summary (Zusammenfassung) | zum Seitenanfang  |
The task of our project work was to test techniques which make it possible to identify fibres (textiles) and to distinguish between them. Anyway the technical expenditure of these methods should be as little as possible.
First we had to find a way how to tell natural from synthetic fibres. For this purpose we carried out the burning-test. For it you have to set every single textile-fibre on fire and to keep an eye on the reaction inside and outside the flame of a burner. Additional you should also pay attention to the smell of the vapour which is built during the burning process. Only natural fibres smell like burned paper (cellulose-fibres, e.g. cotton) or burned horn (protein-fibres, e.g. wool).
After this first step was done we had to search for other techniques which were more specific.
Methods we found were:
- Ninhydrin-reaction and Biuret test to identify the protein in wool and silk,
- the Plumbad-reaction to identify only wool which consists of protein containing sulphur,
- the Beilstein-experiment to identify halogens (e.g. chlorine in PVC-fibres)
We also noticed the different effects of acids, lyes and organic solvents on single textile-fibres. Moreover we heated up fibre samples in test-tubes in order to measure the pH of the escaping vapour. But now it is very important to mention the fact that all experiments listed up above cannot be carried out with mixed fibres but only with pure ones.
After all we have to say that it was really interesting to find out the techniques which made it possible to identify fibres and to tell them apart.
| 7. Anhang | zum Seitenanfang  |
| 7-1. Die Strukturformel von Polymethylmethacrylat (PMMA) | zum Seitenanfang  |
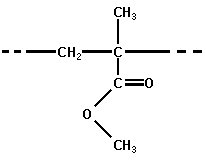
Ausschnitt aus einem Polymethylmethacrylat-Makromolekül
Literatur : [4 ]
| 7-2. Bericht über die erste Projektbesprechung | zum Seitenanfang  |
Am 30.9.04 fand unsere erste Besprechung mit Prof. Schwedt statt. Nach der Begrüßung erklärte Prof. Schwedt uns, dass wir zwischen Naturfaser und Kunstfaser unterscheiden sollen und uns jeweils einige gängige Faserstoffe aussuchen sollen, z.B. Baumwolle, Seide, Wolle, Polyester, Polyamid. Mit diesen Stoffen sollen wir mit einfachen Untersuchungsmethoden prüfen, wie man sie unterscheiden kann. Als Beispiel nannte er uns die Brennprobe z.B. Seide formt sich zu einer Perle und Baumwolle verbrennt wie Papier. Weiter erklärte Prof. Schwedt, dass wir proteinhaltige und nichtproteinhaltige Stoffe voneinander unterscheiden können z.B. mit der Ninhydrin-Probe oder die Reaktion mit Kupfersulfat (Biuret-Reaktion).
Als Literaturhilfe hat Prof. Schwedt uns darauf hingewiesen unter dem Stichwort 'Textilkunde' in der Bibliothek zu schauen. Er hat uns auch vorgeschlagen im 'Römpp Chemielexikon' zu recherchieren, wo wir die Textilien chemisch hinterfragen können, z.B. Herstellung, und auf sein Buch 'Fleckenentfernung', ein Buch über Fleckenmittel, vom Aulis Verlag hingewiesen.
Am Ende der Besprechung angekommen wünschte Prof. Schwedt uns viel Spaß und Erfolg beim Untersuchen.
| 7-3. Bericht über die zweite Projektbesprechung | zum Seitenanfang  |
Am 26.11.04. fand die zweite Besprechung mit Prof. Dr. Schwedt statt. Nachdem wir ihm berichtet haben was wir schon gemacht haben, war er mit unserer Arbeit zufrieden. Prof. Schwedt meinte, dass wir schon genügend Versuche hätten und wir mit dem praktischen Teil schon fertig sind. Des weiteren gab er uns Tipps für die Darstellung in der Dokumentation. Wir sollten die Versuche in einem System der deutlichen Unterscheidung der Textilien einordnen und auch tabellarisch und graphisch gestalten. Da wir Ninhydrin als Sprühreagenz bei der Ninhydrinprobe eingesetzt haben, sagte er uns, dass wir es im Reagenzglas mit etwas Wasser und Textilfaser erwärmen sollen. Nachdem wir nach den Mischfasern gefragt haben, sagte er, dass wir maximal eine Mischfaser wählen sollen und sie untersuchen. Für die Präsentation gab uns Prof. Schwedt den Tipp, einpaar interessante Versuche rauszusuchen und vorzuführen.
| 7-4. Literaturverzeichnis | zum Seitenanfang  |
| [1] | http://aramed.med.uni-rostock.de/lehrbrief/indgifte.htm , 19.01.2005 |
| [2] | Birk, Fritz, Textil- und Warenkunde -2.überarb. Aufl., Verlag Dr. Max Gehlen |
| [3] | Bobeth, Wolfgang (Hrsg.), Textile Faserstoffe -Beschaffenheit und Eigenschaften, Springer -Verlag 1993, Seiten 18-22; 370-375; 382; 384-387 |
| [4] | Boche, Gernot (Hrsg.), Chemie und Gesellschaft: Herausforderung an eine Welt im Wandel; Marburger Forum Philippinum; Umwelt und Medizin Verlagsgesellschaft 1984, Seite 22 |
| [5] | http://www.chemie.fu-berlin.de/chemistry/kunststoffe.htm, 20.01.2005 |
| [6] | http://www.chemie.uni-muenchen.de, 20.01.2005 |
| [7] | http://www.dc2.uni-bielefeld/dc2/plaste/v09.htm, 20.01.2005 |
| [8] | http://de.wikipedia.org/wiki/Baumwolle, 10.01.2005 |
| [9] | http://de.wikipedia.org/wiki/Polyurethan, 21.01.2005 |
| [10] | Elias, Hans-Georg, Makromoleküle Band I -Chemische Struktur und Synthese, 6. vollst. überarb. Aufl., WILEY-VCH Verlag GmbH 1999, Seiten 16;47 |
| [11] | http://www.elly-bk.de/netdays98/s-gesch.htm, 17.01.2005 |
| [12] | http://www.fashion-base.de, 06.10.2004 |
| [13] | http://ff-rohrbach.at/dasfeuer/5.htm, 20.01.2005 |
| [14] | Franck, Adolf, Kunststoff-Kompendium: Aufbau..., Karlheinz Biederbrick. 2. überarb. Aufl., Vogel 1988, Seiten 37; 144; 247-249 |
| [15] | Hofer, Alfons, Stoffe I, 1.Rohstoff: Fasern, Garne und Effekte, 8. vollst. überarb. und erw. Aufl., Deutscher Fachverlag 2000, Seiten 42-43; 592; 714-717 |
| [16] | http://izu.bayern.de/faq/download/kunststoffbrände.pdf, Seiten 21-26, 19.01.2005 |
| [17] | Koslowski, Hans J., Chemiefaser-Lexikon - Begriffe, Zahlen, Handelsnamen. 11. Aufl., Deutscher Fachverlag 1997, Seiten 118-127; 136-137 |
| [18] | Pidde, Jürgen, Handbuch für die Polstertechnik, Hrsg. Bundesinstitut für Berufsbildung, Der Generalsekretär, W. Bertelsmann Verlag 1999 |
| [19] | Rath, Hermann, Lehrbuch der Textilchemie einschließlich der textilchemischen Technologie, 3. neubearb. Aufl., Springer Verlag 1972 |
| [20] | Rogowin, Zakhar Aleksandrovitsch, Hrsg. Albrecht, Wilhelm, Georg Thieme Verlag 1982, Seite 314; 321 |
| [21] | Römpp -Lexikon Chemie, 10. Aufl., Hrsg. J. Falbe und M. Regitz, Georg Thieme Verlag 1999 (Band I-VI), Seiten 3410-3411; 3414-3416; 3441-3442; 3512-3513; 3516-3517; 4478-4479 |
| [22] | Schneider, Wolfgang, Werdegang der Chemie: Entwicklung einer Naturwissenschaft, Haag und Herchen 1999, Seiten 58; 77-78 |
| [23] | http://www.seilnacht.com/Lexikon.htlm, 19.01.2005 |
| [24] | http://www.theochem.uni-duisburg.de/DC/material/silicon/versuch/versuch6.htm, 18.01.2005 |
| [25] | http://uni-bayreuth.de/departments/didaktikchemie/umat/fasern_syn.htm, 10.01.05 |
| [26] | http://www.uni-bayreuth.de/departments/didaktikchemie/umat/ninhydrin.htm, 17.01.2005 |
>> Diese Projektarbeit komplett downloaden / ausdrucken (in PDF)
« zurück zur Übersicht - Projektarbeiten

