« zurück zur Übersicht - Wettbewerb Umweltfreundlicher Chemieunterricht
 Wettbewerb Umweltfreundlicher Chemieunterricht
Wettbewerb Umweltfreundlicher Chemieunterricht
Beitrag des Wettbewerbes 2000:
Chemie mit dem blauen Farbstoff der Smarties - Projektarbeit mit einem Leistungskurs Chemie
Martin Ratermann, Liebfrauenschule Vechta (Preisträger)
als PDF-Datei (185 KB)
|
1. Vorwort 2. Patentblau V als pH-Indikator 3. Reaktion von Patentblau V mit Natronlauge 4. Reaktionskinetik mit blauen Smarties? 5. Schluss Liste der verwendeten Literatur |
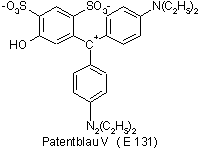 Im Chemieunterricht erfreuen sich Untersuchungen von Farbstoffen großer Beliebtheit. Naheliegend ist in diesem Zusammenhang die Untersuchung gefärbter Lebensmittel. Leicht zu untersuchende Objekte sind z.B. bunte Schokolinsen. Wir hatten bereits die Farbstoffe in Produkten verschiedener Hersteller isoliert und untersucht, als wir auf interessante Beobachtungen stießen. Da wir uns ein Halbjahr lang mit dem Thema Reaktionskinetik und chemisches Gleichgewicht beschäftigt hatten, fiel uns auf, dass der blaue Farbstoff der Smarties, Patentblau V1, ebenso zu den Triarylmethanfarbstoffen gehört wie etwa das Kristallviolett, dessen Entfärbungsreaktion mit Natronlauge zu den Standardreaktionen für kinetische Untersuchungen zählt. Freihandversuche ergaben, dass Patentblau V einen pH-abhängigen Farbwechsel zeigt und sich bei Zugabe von Natronlauge sehr langsam entfärbt. Bereits in einer früheren Arbeit2 hatte sich einer meiner Leistungskurse erfolgreich mit der Chemie verschiedener Triarylmethanfarbstoffe beschäftigt. Deshalb schien es uns interessant und erfolgversprechend, die Chemie des Patentblau V näher zu untersuchen. Patentblau V ist als zugelassener Lebensmittelfarbstoff ein absolut unbedenklicher Stoff für den Chemieunterricht. Alle Experimente wurden zudem im Mikromaßstab durchgeführt, so dass der Verbrauch an Chemikalien extrem gering war und praktisch keine Entsorgungsprobleme auftraten.
Im Chemieunterricht erfreuen sich Untersuchungen von Farbstoffen großer Beliebtheit. Naheliegend ist in diesem Zusammenhang die Untersuchung gefärbter Lebensmittel. Leicht zu untersuchende Objekte sind z.B. bunte Schokolinsen. Wir hatten bereits die Farbstoffe in Produkten verschiedener Hersteller isoliert und untersucht, als wir auf interessante Beobachtungen stießen. Da wir uns ein Halbjahr lang mit dem Thema Reaktionskinetik und chemisches Gleichgewicht beschäftigt hatten, fiel uns auf, dass der blaue Farbstoff der Smarties, Patentblau V1, ebenso zu den Triarylmethanfarbstoffen gehört wie etwa das Kristallviolett, dessen Entfärbungsreaktion mit Natronlauge zu den Standardreaktionen für kinetische Untersuchungen zählt. Freihandversuche ergaben, dass Patentblau V einen pH-abhängigen Farbwechsel zeigt und sich bei Zugabe von Natronlauge sehr langsam entfärbt. Bereits in einer früheren Arbeit2 hatte sich einer meiner Leistungskurse erfolgreich mit der Chemie verschiedener Triarylmethanfarbstoffe beschäftigt. Deshalb schien es uns interessant und erfolgversprechend, die Chemie des Patentblau V näher zu untersuchen. Patentblau V ist als zugelassener Lebensmittelfarbstoff ein absolut unbedenklicher Stoff für den Chemieunterricht. Alle Experimente wurden zudem im Mikromaßstab durchgeführt, so dass der Verbrauch an Chemikalien extrem gering war und praktisch keine Entsorgungsprobleme auftraten.
2. Patentblau V als pH-Indikator![]()
2.1 Absorptionsverhalten von Patentblau V
Beim Zutropfen von Salzsäure zu einer Lösung von Patentblau konnte ein Farbwechsel von blau nach gelb beobachtet werden. Dieser Farbwechsel sollte quantitativ untersucht werden. Als Methode bot sich die Photometrie an. Zunächst wurde ein Absorptionsspektrum von Patentblau V3 in neutraler wässeriger Lösung ermittelt4.
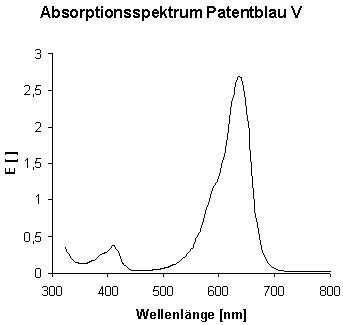
Das Absorptionsspektrum von Patentblau V zeigt ein Absorptionsmaximum bei 639 nm. Dies entspricht dem Literaturwert5. Die später folgenden kinetischen Untersuchungen wurden bei dieser Wellenlänge durchgeführt.
Die beim Ansäuern entstehende gelbe Form des Farbstoffes absorbiert oberhalb 600 nm nicht. Dies wurde für die folgenden Untersuchungen zum Farbwechsel von Patentblau ausgenutzt.
2.2 Bestimmung des pKs-Wertes von Patentblau V
Für die Untersuchung des Farbwechsels wurden jeweils 9 ml Lösungen verschiedener pH-Werte angesetzt. Zu diesen Lösungen wurde jeweils 1 ml einer Patentblaulösung gegeben. Nach Zugabe der Patentblaulösung wurde der pH-Wert exakt bestimmt. Anschließend wurden von allen Lösungen Absorptionsspektren gefahren.
Beim Ansäuern der Lösung kommt es zu einer Protonierung zumindest eines der Stickstoffatome. Dadurch erfolgt eine Desaktivierung eines der Auxochrome, und folglich kommt es zu einer Farbverschiebung.
Absorption von Patentblau V bei unterschiedlichen pH-Werten:
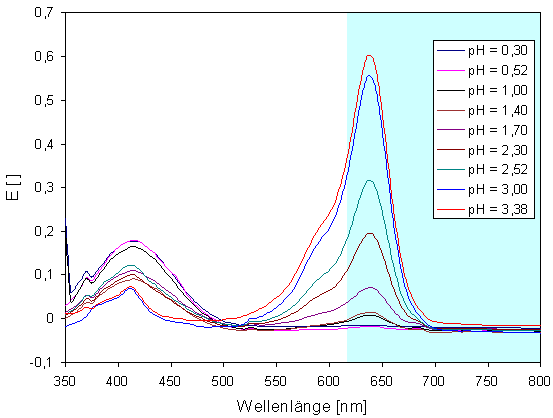
Die Abbildung zeigt, dass mit niedriger werdendem pH-Wert die Absorption bei 639 nm sinkt. Dafür nimmt die für gelbe Farbstoffe typische Absorption zwischen 400 und 450 nm zu. Die quantitative Analyse der jeweils noch vorhandenen Anteile an gelber und blauer Form ermöglicht die Ermittlung des pKs-Wertes von Patentblau. Der pKs-Wert ist der pH-Wert, bei dem blaue und gelbe Form in gleichen Anteilen vorliegen.
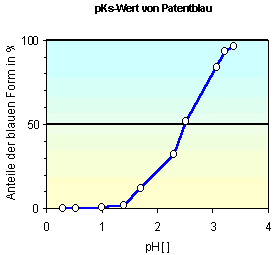
Für Patentblau V ergibt sich ein pKs-Wert von 2.5. Die Acidität des Farbstoffes ist damit etwas geringer als die vergleichbarer Triarylmethan-farbstoffe wie Brillantgrün oder Kristallviolett. Dies wird verständlich, wenn man davon ausgeht, dass die Sulfonsäuresubstituenten und die Hydroxylgruppe elektronenschiebende Wirkungen haben6. Dadurch wird die Basizität der Stickstoffatome erhöht, und die Acidität herabgesetzt.
3. Reaktion von Patentblau V mit Natronlauge![]()
3.1. Zusammenhang zwischen Extinktion und Konzentration
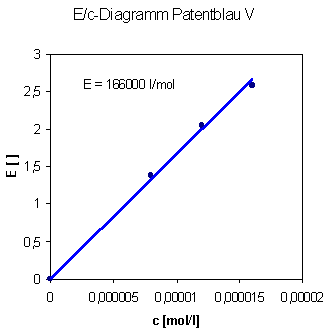
Vorversuche hatten ergeben, dass sich Patentblaulösungen bei Zugabe von Natronlauge langsam entfärbten. Diese Reaktion sollte photometrisch verfolgt werden. Als vorbereitende Untersuchung wurde der Zusammenhang zwischen Extinktion und Konzentration des Farbstoffes untersucht. Dazu wurde eine Verdünnungsreihe mit Patentblau-lösungen von Konzentrationen kleiner als 2 x 10-5 mol/l angelegt. Das E/c-Diagramm ergab eine Ursprungsgerade. Im untersuchten Konzentrationsbereich ist also die Patentblaukonzentration der Extinktion proportional. Das Lambert-Beer`sche Gesetz
![]()
gilt mit ![]() = 166000 l/mol.
= 166000 l/mol.
Parallel zu den Versuchen mit dem gekauften Farbstoff wurde probiert, blaue Smarties selbst für die Experimente einzusetzen. Dazu wurden in einer Versuchsreihe ein bis 6 Smarties in je 100 ml Wasser gegeben und kurz geschüttelt. Anschließend wurde zügig filtriert. Die blauen Lösungen wurden ebenfalls bei einer Wellenlänge von 639 nm photometrisch untersucht. Dabei wurden erstaunlich genaue Daten erhalten.
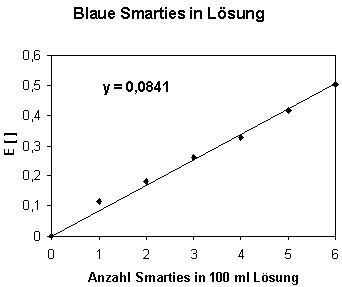
Legt man den oben ermittelten Zusammenhang zwischen Extinktion und Konzentration von Patentblau zu Grunde, ergibt sich, dass jede blaue Schokolinse recht exakt 5 x 10-8 mol Patentblau enthält. Mit blauen Smarties können folglich ziemlich genau Lösungen mit definierter Patentblau-konzentration hergestellt werden.
3.2 Entfärbungsreaktion von Patentblau mit Natronlauge![]()
In früheren Versuchsreihen hatte ich bereits mit Kursen Entfärbungsreaktionen verschiedener Triarylmethanfarbstoffe untersucht1. Diese Reaktionen waren jeweils nach wenigen Minuten beendet gewesen. Vorversuche zeigten, dass die Entfärbung von Patentblau selbst bei höheren Natronlaugekonzentrationen mehrere Stunden dauerte. Diese Entfärbungsreaktion ließ sich nur durch den Einsatz des Computers7 sinnvoll verfolgen. Vormittags wurden dazu die Messungen angesetzt und am darauffolgenden Tag beendet und ausgewertet. Für jeden Versuchsansatz wurden 1,5 ml Patentblaulösung der Konzentration 2 x 10-5 mol/l und 1,5 ml Natronlauge unterschiedlicher Konzentrationen eingesetzt. Die Messungen erfolgten wie gewohnt bei einer Wellenlänge von 639 nm.
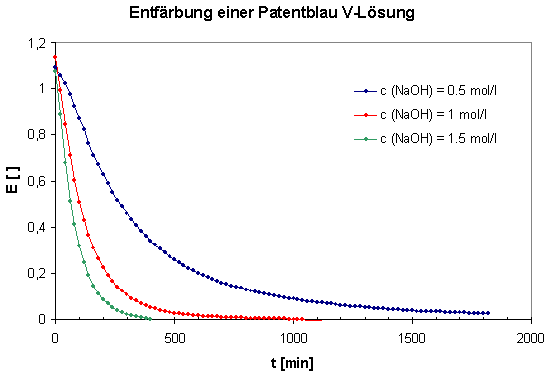
3.3 Reaktionsordnung der Patentblau V-Entfärbung
Das E/t-Diagramm zeigt, dass vielversprechende Messwerte erhalten wurden. Bezüglich der Kinetik der Reaktion war anzunehmen, dass es sich wie bei den früher untersuchten Reaktionen von Triarylmethanfarbstoffen um Reaktionen pseudo-1.Ordnung handeln sollte. Dies konnte durch ln E/t-Diagramme belegt werden. Wie für Reaktionen 1.Ordnung zu fordern ergaben sich hier lineare Zusammenhänge. Anhand der erhaltenen Geraden ließen sich die Geschwindigkeitskonstanten pseudo-1.Ordnung ermitteln.
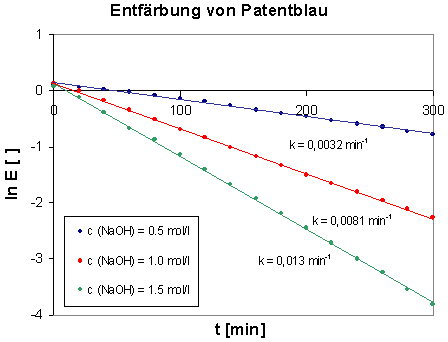
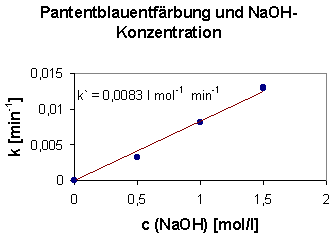 Mit dem nebenstehenden Diagramm ließ sich zeigen, dass die Geschwindigkeit der Reaktion ebenso wie von der Patentblaukonzentration von der Natronlaugekonzentration abhängt. Es handelt sich also um eine Reaktion pseudo-1. Ordnung. Damit gilt der folgende Zusammenhang zwischen Reaktionsgeschwindigkeit und Konzentrationen:
Mit dem nebenstehenden Diagramm ließ sich zeigen, dass die Geschwindigkeit der Reaktion ebenso wie von der Patentblaukonzentration von der Natronlaugekonzentration abhängt. Es handelt sich also um eine Reaktion pseudo-1. Ordnung. Damit gilt der folgende Zusammenhang zwischen Reaktionsgeschwindigkeit und Konzentrationen:
v = k x cPB x cNaOH
mit k = 0,0083 l x min-1 x mol-1
Der Vergleich der ermittelten Geschwindigkeitskonstante mit den für andere Triarylmethanfarbstoffe ermittelten Daten8 zeigt, dass sich Patentblau um einige Größenordnungen langsamer mit Natronlauge entfärben lässt.
| Triarylmethanfarbstoff | k (zweiter Ordnung) [l/min x mol] |
| Patentblau V | 0.0083 |
| para-Fuchsin | 87.45 |
| Kristallviolett | 4.39 |
| Ethylviolett | 1.73 |
| Malachitgrün | 38.18 |
| Brillantgrün | 23.60 |
Begründung des abweichenden Reaktionsverhaltens von Patentblau V: Vergleicht man den Aufbau des Patentblaumoleküls mit dem der anderen Triarylmethanfarbstoffe, fallen besonders folgende Unterschiede auf: Dabei ist ein Vergleich mit Brillantgrün am einfachsten.
- Das Patentblaumolekül trägt zusätzlich zwei Sulfonsäuregruppen und ist in der gefärbten Form dadurch insgesamt einfach negativ geladen. Alle anderen in der Tabelle genannten Triarylmethanfarbstoffmoleküle sind jeweils einfach positiv geladen.
- Das Patentblaumolekül trägt zusätzlich eine Hydroxylgruppe.
Die Entfärbungsreaktion besteht in einer Anlagerung eines Hydroxidions an das zentrale, positiv teilgeladene Kohlenstoffatom. Dabei wird das farbgebende mesomere System zerstört. Bereits die Untersuchung der anderen Triarylmethanfarbstoffe hatte gezeigt, dass elektronenschiebende Reste den Elektronenmangel am zentralen Kohlenstoffatom partiell ausgleichen. Dadurch wird die Affinität zwischen Hydroxidion und zentralem C-Atom erniedrigt und die Reaktion verlangsamt. Sowohl Sulfonsäuregruppen als auch die Hydroxidgruppe haben über ihre +M-Effekte elektronenschiebende Wirkungen. Dies trägt dazu bei, die Entfärbungsreaktion von Patentblau zu verlangsamen.
Anders als bei den anderen Triarylmethanfarbstoffen müssen sich Hydroxidionen beim Patentblau V einem negativen Teilchen nähern. Die ist sicherlich ungünstiger und findet deshalb auch seltener statt. Auch dies trägt zusammen mit der damit verbundenen Erhöhung der negativen Ladung des Farbstoffions zu einer geringeren Reaktionsgeschwindigkeit bei.
3.4 Reaktionsgeschwindigkeit und Lösungsmittelpolarität![]()
Für Kristallviolett ist in der Schulbuchliteratur beschrieben, wie die Lösungsmittelpolarität das Reaktionsverhalten beeinflusst9. Es sollte untersucht werden, ob entsprechende Zusammenhänge auch für die Reaktion von Patentblau V mit Natronlauge gelten. Dazu wurden unterschiedliche Anteile des Wassers durch das weniger polare Methanol10 ersetzt.
| Wasser | Methanol | Patentblau |
| 1.5 ml | 0 ml | 1.5 ml |
| 1.2 ml | 0.3 ml | 1.5 ml |
| 0.9 ml | 0.6 ml | 1.5 ml |
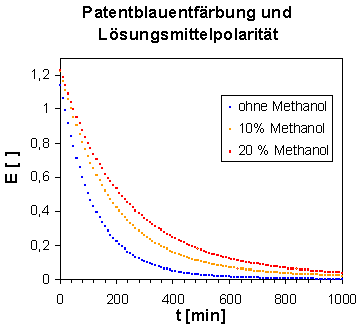
Bereits das E/t-Diagramm zeigt eindeutig, dass die Reaktion um so langsamer abläuft, je höher der Anteil an Methanol, je unpolarer das Lösungsmittelgemisch also ist. Für Kristallviolett ist in der Literatur ein genau umgekehrter Zusammenhang beschrieben. Dieser wurde von uns im Unterricht bestätigt.
Begründung des Lösungsmitteleinflusses: Unpolare Lösungsmittel begünstigen das Verschwinden von Ladungen. Bei der Reaktion von Kristallviolett mit Hydroxidionen verschwinden in der Tat Ladungen. Dies ist bei der Patentblauentfärbung nicht der Fall. Die Ladung des Farbstoffions selbst nimmt sogar zu. Wenn auch der Lösungsmitteleinfluss damit nicht vollständig erklärbar ist, so wird doch verständlich, dass die Polarität des Lösungsmittels beim Patentblau einen anderen Einfluss hat als beim Kristallviolett.
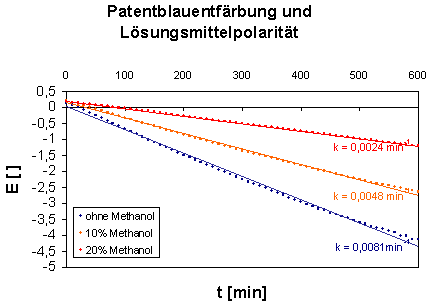
Die weitergehende Analyse der Ergebnisse der Patentblauentfärbung zeigte, dass die veränderte Lösungsmittelzusammensetzung keinen Einfluss auf die Reaktionsordnung hat. Das ln E/t-Diagramm belegt, dass unverändert eine Kinetik pseudo-1. Ordnung vorliegt.
3.5 Patentblauentfärbung und Temperatur![]()
Der Einfluss der Temperatur auf die Geschwindigkeit der Entfärbungsreaktion sollte quantitativ untersucht werden. Wir verfügen in unserer Sammlung über ein einfaches Selbstbau-Photometer11, mit dem es möglich ist, die Entfärbung blauer Lösungen bei unterschiedlichen Temperaturen zu untersuchen. Auch dieses Photometer lässt sich über einen Spannungsausgang mit dem PC verbinden, da dass bequeme Messungen möglich sind. Bei höheren Temperaturen ist zu beobachten, dass die Entfärbungsreaktion nach wenigen Minuten beendet ist. Für unterschiedliche Temperaturen wurden die folgenden Geschwindigkeitskonstanen ermittelt. Eingesetzt wurde jeweils Natronlauge der Konzentration 1 mol/l.
| Temperatur [°C] | T [K] | k [l x mol-1 x min-1] |
| 35.0 | 308.15 | 0.0081 |
| 48.6 | 321.75 | 0.0280 |
| 54.0 | 327.15 | 0.0300 |
| 70.0 | 343.15 | 0.1350 |
| 85.8 | 358.95 | 0.3750 |
| 87.0 | 360.15 | 0.4260 |
| 90.0 | 363.15 | 0.5160 |
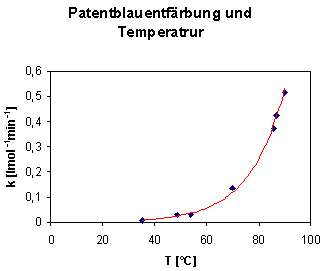
Das k/T-Diagramm zeigt den erheblichen Einfluss der Temperatur auf die Reaktionsgeschwindigkeit. Wie die rot dargestellte exponentielle Kurve zeigt, ist eine exponentielle Abhängigkeit der Reaktionsgeschwindigkeit von der Temperatur anzunehmen.
3.6 Ermittlung der Aktivierungsenthalpie der Patentblauentfärbung![]()
Nach Arrhenius besteht für chemische Reaktionen folgender Zusammenhang zwischen Temperatur und Geschwindigkeitskonstante:
k = A x e-EA/(R x T)
bzw. in logarithmischer Darstellung:
ln k = ln A - EA/(R x T)
mit k = Geschwindigkeitskonstante
A = Arrheniuskonstante
EA = Aktivierungsenthalpie
R = Rydberg-Konstante = 8.314 J/(K x mol)
T = Temperatur in K
Folglich sollte das ln k / 1/T - Diagramm eine Gerade mit der Steigung -EA/R ergeben, aus der sich die Aktivierungsenthalpie EA ermitteln lässt.
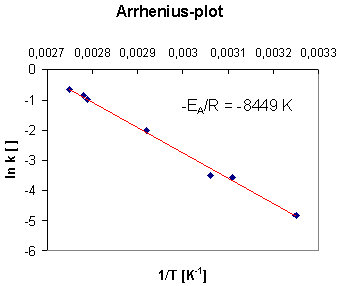
| Für die Aktivierungenethalpie EA ergibt sich: EA | = 8449 K x R |
| = 8449 K x 8.314 J/(K x mol) = 70245 J/mol = 70.2 kJ/mol |
4. Reaktionskinetik mit blauen Smarties?![]()
Nachdem wir die beschriebenen Experimente mit guten Ergebnissen durchgeführt hatten, lag es nahe zu versuchen, blaue Smarties direkt für kinetische Untersuchungen einzusetzen. Immerhin hatten die Experimente zum Zusammenhang zwischen Extinktion und Konzentration12 ergeben, dass man mit Smarties genau konzentrierte Lösungen von Patentblau herstellen konnte.
Aufgrund eigener chromatographischer Untersuchungen war uns bekannt, dass blaue Snarties neben Patentblau V einen weiteren roten Farbstoff enthalten. Das Absorptionsspektrum des blauen Smarties-Extraktes unterscheidet sich jedoch praktisch nicht von dem einer reinen Patentblau V-Lösung. Der enthaltene rote Farbstoff absorbiert im Bereich von 639 nm sicher nicht, so dass wir annahmen, mit unserer Analytik die Entfärbung des blauen Smarties-Farbstoffes ungestört untersuchen zu können.
Wir haben einige mit blauen Smarties hergestellte Lösungen entfärbt und sind dabei absolut reproduzierbar auf interessante, zum Teil unerwartete Ergebnisse gestoßen.
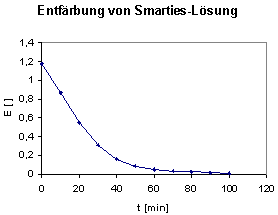 Das E/t-Diagramm zeigt, dass die Entfärbunbgsreaktion bereits nach etwa 100 Minuten beendet ist. Die Reaktion verläuft also wesentlich schneller, wenn statt des reinen Farbstoffes Patentblau V das aus den Schokolinsen herausgelöste Gemisch verwendet wird. Da dieses ergebnis auch für uns überraschend war, haben wir das Experiment mehrfach mit immer gleichem Ergebnis wiederholt.
Das E/t-Diagramm zeigt, dass die Entfärbunbgsreaktion bereits nach etwa 100 Minuten beendet ist. Die Reaktion verläuft also wesentlich schneller, wenn statt des reinen Farbstoffes Patentblau V das aus den Schokolinsen herausgelöste Gemisch verwendet wird. Da dieses ergebnis auch für uns überraschend war, haben wir das Experiment mehrfach mit immer gleichem Ergebnis wiederholt.
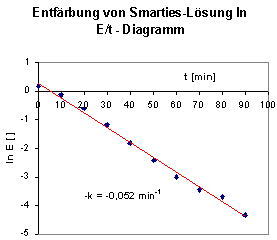 Das ln E/t-Diagramm zeigt, dass es bei einer Kinetik pseudo-1.Ordnung bleibt. Plausible Gründe für das abweichende Verhalten des dirkekt aus Smarties gewonnenen Farbstoffes konnten wir noch nicht finden. Zur Zeit scheint uns eine katalytische Wirkung der neben dem Farbstoff in Lösung befindlichen Substanzen aus den Schokolinsen die einzig mögliche Begründung dieses überraschenden Effektes zu sein.
Das ln E/t-Diagramm zeigt, dass es bei einer Kinetik pseudo-1.Ordnung bleibt. Plausible Gründe für das abweichende Verhalten des dirkekt aus Smarties gewonnenen Farbstoffes konnten wir noch nicht finden. Zur Zeit scheint uns eine katalytische Wirkung der neben dem Farbstoff in Lösung befindlichen Substanzen aus den Schokolinsen die einzig mögliche Begründung dieses überraschenden Effektes zu sein.
Nachdem wir unsere Versuche durchgeführt hatten, waren wir sehr erfreut und auch etwas überrsascht, mit welcher Präzision sich die Chemie des Farbstoffes Patentblau V untersuchen ließ. Weitere Versuche zeigten, dass alle beschriebenen Ergebnisse sind absolut reproduzierbar sind.
Es zeigte sich, dass durch den Einsatz eines Computers Experimente zugänglich werden, die ohne einen Rechnereinsatz nicht durchführbar wären, in diesem Fall wegen der langen Versuchszeiten. Dadurch werden Freiräume geschaffen, auch einmal Dinge zu untersuchen, die bisher nicht in Lehrbüchern beschrieben sind. Wer bereits einmal Reaktionskinetik ohne Rechner betrieben hat, kann einschätzen, wie umfangreich die notwendigen Auswertungen werden. Mit geeigneter Software sind die umfangreichen Daten (manchmal einige Tausend Messwerte) in Minuten zu verarbeiten. So macht auch Kinetik Spaß!
Wir hatten nach unseren Experimenten mit dem gekauften Patentblau V eigentlich erwartet, dass sich der aus Smarties herausgelöste und nicht gereinigte Farbstoff entsprechend verhalten sollte. Die Tatsache, dass die Reaktivität von der des Reinstoffes abwich zeigt, dass sich im Verlauf solcher kleinerer Forschungsprojekte ständig neue Fragestellungen ergeben. Andrerseits besteht die Möglichkeit mit blauen Smarties die Gültigkeit des lambert-Beer`schen Gesetztes nachzuweisen und eine Kinetik pseudo-1.Ordnung zu erarbeiten. Es ist zu erwarten, dass sich mit dem Farbstoff aus den Schokolinsen auch die anderen in dieser Arbeit beschriebenen Effekte nachweisen lassen.
Insgesamt hat sich eine solche Fülle an geeigneten Experimenten für einen Oberstufenkurs ergeben, dass es möglich erscheint, einen großen Teil eines Kursthemas "Reaktionskinetik" mit diesen Experimenten zu bestreiten.
Der Verbrauch an Chemikalien ist dabei minimal. Es werden lediglich einige Milliliter Lösung des völlig unbedenklichen Lebensmittelfarbstoffes Patentblau V in extrem geringer Konzentration und einige Milliliter Natronlauge benötigt, dazu zur Untersuchung der pH-Abhängigkeit der Farbe wenige Milliter Salzsäure und verschiedener Pufferlösungen. Die geringe Menge des für die Untersuchung des Lösungemitteleffektes eingesetzten giftigen Methanols (etwa 2 ml) scheint uns vertretbar. Wir werden aber weiterhin überprüfen, ob ein Ersatz möglich ist.
Liste der verwendeten Literatur:![]()
- DFG Farbstoffe für Lebensmittel; VCH-Verlagsgesellschaft mbH, 1988
- Fluka-Katalog 1999/2000
- Lang,G.: Reaktionskinetik, Diesterweg-Verlag, Frankfurt 1990
- Ratermann, Martin: Substituenteneffekte auf die Geschwindigkeiten der Entfärbungsreaktionen von Triarylmethanfarbstoffen, in: Chemie in der Schule, Sonderheft zum Wettbewerb Umweltfreundlicher Chemieunterricht 1996
- Wittke, Georg: Farbstoffchemie, Diesterweg-Verlag, Frankfurt 1992
Folgende Schüler*innen waren an den Untersuchungen beteiligt:
Liebfrauenschule Vechta, Leistungskurs Chemie, Jahrgangsstufe 12, Schuljahr 1999/2000
Fachlehrer: Martin Ratermann, E-mail: Martin.Ratermann@t-online.de
Alfschnieder, Rebecca; Baumann, Sabrina; Boeckmann, Kathrin; Button, Chrysta, Hachmöller, Markus; Hartmann, Meike; Meißner Nathalie; Meyer, Elisabeth; Rütemann, Sonja; Schumacher, Ruth; Spille, Sarah; Staerk, Isabelle
- Strukturformel erstellt mit ISIS DRAW
- Ratermann, Martin: Substituenteneffekte auf die Geschwindigkeiten der Entfärbungsreaktionen von Triarylmethanfarbstoffen, in: Chemie in der Schule, Sonderheft zum Wettbewerb Umweltfreundlicher Chemieunterricht 1996
- Fluka Best.Nr: 76270
- Eingesetzt wurde ein Photometer Typ Novaspec II mit Software UNIMESS des AK Computer im Chemieunterricht.
- vgl. Literaturstelle 1 im Anhang
- vgl. Kap. 3.3
- Verwendet wurde ein Photometer Typ Novaspec II. Dieses wurde direkt mit dem PC verbunden. Die Software UNIMESS des AK Computer im Chemieunterricht wurde eingesetzt.
- Ratermann, Martin: Substituenteneffekte auf die Geschwindigkeiten der Entfärbungsreaktionen von Triarylmethanfarbstoffen, in: Chemie in der Schule, Sonderheft zum Wettbewerb Umweltfreundlicher Chemieunterricht 1996
- vgl. Lang: Reaktionskinetik: Diesterweg-Verlag, Frankfurt 1990, S. 17 f.
- Es wurde der Versuch unternommen, statt Methanol weniger giftige Substanzen einzusetzen. Bisher konnte jedoch kein geeigneter Ersatzstoff gefunden werden. Die Suche geht weiter.
- Das Photometer wurde von Herrn Frühling, Hochschule Vechta, gebaut.
- vgl. Kap. 3.1
zur Übersicht über die Beiträge des Wettbewerbes 2000

