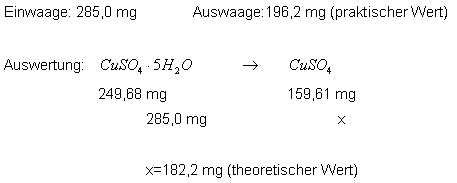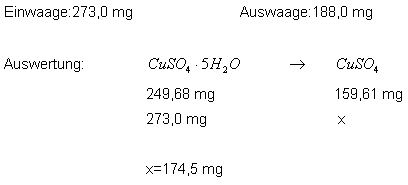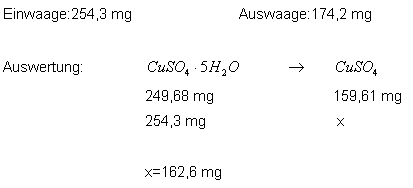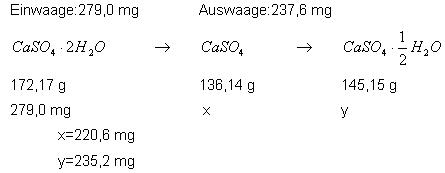« zurück zur Übersicht - Projektarbeiten
"Schulversuche in der Mikrowelle"
von Stephanie Korff (Schuljahr 2007/08)
| 1. Zusammenfassung | zum Seitenanfang  |
Meine Projektarbeit umfasst das Thema "Schulversuche in der Mikrowelle". Diese Versuche werden bereits im Fehling Lab mit Schülern und Lehrern getestet. Meine Aufgabe war es, diese Versuche zu optimieren. In einigen Fällen ist es mir gelungen, eine Optimierung zu erzielen. Andere Versuche waren so simpel, dass meiner Meinung nach nichts optimiert werden konnte.
Weiterhin gehörte es zu meinen Aufgaben neue Versuche und Synthesen, die keine giftigen Chemikalien enthalten und so für Schüler*innen geeignet sind, zu finden. Unter diesem Aspekt gelang es mir, Fluoreszein und einen Polyester aus Citronensäure und Rizinusöl in der Mikrowelle herzustellen. Ich ließ in einem anderen Versuch ein Playmobilmännchen schmelzen und stellte eine Handcreme mit verschiedenen Aromastoffen in der Mikrowelle her.
| 2. Summary | zum Seitenanfang  |
My project work includes the theme of "education experiments in the microwave". These trials are already in Fehling Lab with students and teachers tested. My task was to optimize these experiments. In some cases I succeeded an optimization. Other attempts were so simple that I think nothing could be optimized.
Furthermore, it belonged to my duties to find new tests and syntheses, which contain no toxic chemicals and so are suitable for students. Under this aspect, I synthesized Fluorescin and a polyester from citric acid and castor oil in the microwave. In another attempt I melt a Playmobil figure and placed a hand cream with various aromatic substances in the microwave.
| 3. Einleitung | zum Seitenanfang  |
Das Thema umfasst Schülerversuche in der Mikrowelle. Da die Mikrowelle in der analytischen Chemie immer wichtiger von Bedeutung wird, wird auch überlegt, die Mikrowelle in den Laboralltag eines Chemieschülers bzw. Chemieauszubildenden einzubauen. Die Mikrowelle hat gerade für Synthesen einige Vorteile gegenüber dem üblichen Erhitzen auf dem Brenner oder der Heizplatte.
Durch die Mikrowellen werden höhere Reaktionsausbeuten erzielt und kurze Reaktionszeiten benötigt. Jedoch muss durch die schnelle Reaktion und rasche Erhitzung darauf geachtet werden, dass keine unerwünschten Nebenreaktionen auftreten oder das Präparat sogar zerstört wird.
| 4. Die Mikrowelle | zum Seitenanfang  |
| 4-1. Geschichte der Mikrowelle | zum Seitenanfang  |
Ein Mikrowellenherd ist ein Gerät zum schnellen Erhitzen von Flüssigkeiten, Speisen oder anderen geeigneten Stoffen mithilfe der Absorption von Mikrowellen.
Der amerikanische Ingenieur Percy Spencer entdeckte per Zufall, dass mit Mikrowellen Essen erwärmt werden kann. Er arbeitete in diesem Moment an Magnetrons für die Firma Raytheon, als in seiner Hosentasche sein Schokoriegel aufgrund der Mikrowellenstrahlen schmolz. Überrascht von dieser Entdeckung forschte er weiter und untersuchte die Wirkung der Strahlen auf Popcorn. Popcorn war so das erste in der Mikrowelle zubereitete Nahrungsmittel.
1946 ließ Raytheon den ersten Mikrowellenherd patentieren und 1947 bauten sie das erste Exemplar, welches jedoch 340kg schwer war und fast 1,80m hoch. Es hatte eine Leistung von 3000 Watt und besaß eine Wasserkühlung.
1954 kam die erste kommerzielle Mikrowelle mit einer Leistung von 1600 Watt für etwa 2000 $ auf den Markt.
1965 kamen die Haushaltsmikrowellen für etwa 500 $ auf den Markt.
Da in den 1970er Jahren der Preis für eine Mikrowelle sank, stiegen die Verkaufszahlen rapide an und ungefähr 40 000 Geräte wurden in den USA verkauft.
Fünf Jahre später waren es bereits 1 Millionen.
| 4-2. Einsatz der Mikrowelle | zum Seitenanfang  |
Im 2.Weltkrieg zunächst in der Nachrichtentechnik. Die Hochfrequenzstrahlen waren wichtig bei Radar und Richtfunk.
In der Lebensmittelindustrie zum Auftauen von Fleisch, Früchten oder Gemüse, etc. Ebenfalls zum Sterilisieren von u.a. Milch und Bier.
Die Nährstoffverluste sind vergleichbar mit denen durch herkömmliches Kochen.
Die Mikrowelle in der Küche hat die Vorteile, dass das Kochen einfacher ist und eine Menge Zeit spart. Jedoch fördern Mikrowellenherde den Trend zur Fertigkost und die darin zubereitete Nahrung soll auf Dauer der Gesundheit schaden.
Diese Tücken der Mikrowelle wurden in einem russischen Experiment in den '70 er Jahren verdeutlicht: Nahrungsbestandteile wie Eiweiße oder Glykoside zerfallen widernatürlich. Weiterhin entstanden in Milch und Getreide neue, krebserregende Verbindungen; in anderen pflanzlichen Produkten entstanden vermehrt freie Radikale. Die Folge davon sind unter anderem Verdauungsbeschwerden, Zunahme der Krebszellen im Blutserum und Funktionsstörrungen im Lymphsystem.
1991 machten Hans Hertel und Bernhard Blanc eine Studie. Die Versuchspersonen zeigten nach dem Genuss von Mikrowellennahrung Veränderungen im Blutbild, die das Anfangsstadium eines Krebsgeschehens anzuzeigen scheint.
| 4-3. Mikrowellenstrahlung | zum Seitenanfang  |
Elektromagnetische Strahlung erfolgt im Frequenzbereich von 300 MHz bis 300 GHz. Dies entspricht der Wellenlänge von 1m bis 1mm. Die Mikrowelle besitzt eine Frequenz von 2,45 GHz.
Freie Moleküle absorbieren elektromagnetische Wellen durch Anregung von Schwingungen und Rotation. Bei Wasser sind Schwingungen und Rotation eingeschränkt. Wasser hat aufgrund seines Dipolmoments einen Teil an dissozierten Molekülen und eine gewisse Leitfähigkeit. Die Moleküle in flüssiger oder fester Materie werden durch das elektrische Feld polarisiert und die schon polarisierten Moleküle ausgerichtet. Die polaren Wassermoleküle sind in der Speise bereits polarisiert. Dies führt zu Schwingungen und Rotation der Moleküle, sodass sich das Wasser erwärmt. Eis kann nur schlecht erwärmt werden, da die Wassermoleküle im Kristallgitter unbeweglich sind. Auf diese Weise wird nur das bereits geschmolzene Wasser erwärmt, welches dann das Eis zum Schmelzen bringt.
| 4-4. Die Bestandteile einer Mikrowelle | zum Seitenanfang  |
Das Gehäuse stellt einen Faradayschen Käfig dar; das bedeutet, dass nur im Innenraum Mikrowellenstrahlen sich aufgrund der metallischen Wände, die die Strahlen optimal reflektieren, verteilen. Der Außenraum bleibt daher feldfrei.
Die Glastür besteht außen aus Glas und innen aus einem Metallgitter. Dadurch wird der Anwender von den Mikrowellenstrahlen geschützt und kann aber gleichzeitig das Gargut betrachten. Das Gitter wirkt wie eine Metallplatte, denn die Strahlen können nicht austreten, da die Wellenlänge der Strahlung größer ist als die Maschenweite des Gitters. Die Mikrowelle darf unter keinen Umständen bei geöffneter Tür arbeiten.
Im Garraum befindet sich das Mikrowellengeschirr, das meistens aus Glas oder Kunststoff besteht, da beide Stoffe die Strahlung nicht reflektieren.
Der Drehteller besteht aus Glas und dreht sich während der Bestrahlung im Kreis. Dadurch wird die Speise oder die zu erhitzende Substanz gleichmäßig erhitzt.
Das Magnetron erzeugt die Mikrowellenstrahlen. In ihm ist die Kathode (zylinderförmig) von der Anode (ringförmig) umgeben. Die Anode besteht aus einem Anodenblock, in dem breite Schlitze und Bohrungen eingebaut sind, sodass eine definierte Frequenz ausgebildet werden kann.
Zwischen Kathode und Anode werden 4000 Volt angelegt. Dadurch erhält man ein elektrisches Feld. Zwei Magnete erzeugen senkrecht dazu ein magnetisches Feld. Durch die Wirkung beider Felder werden Elektronen um die Kathode abgelenkt.
Die Elektronen erzeugen dabei eine elektrische Schwingung von 2,45 GHz (dies entspricht Wellen mit einer Wellenlänge von 12 cm), die dann in den Hohlleiter gelangt und in dem Garraum überführt wird.Der Hohlleiter ist die Verbindung zwischen Magnetron und Garraum; er besteht aus einem metallischen Hohlkörper. Der Hohlleiter ist an die Wellenlängen angepasst, sodass keine Mikrowellenstrahlen verloren gehen.
Das Kühlgebläse dient zur Kühlung des Magnetrons, da sehr viel Wärmeenergie entsteht. Die verlorene Wärme wird durch Schlitze ins Freie geleitet.
In dem Transformator wird eine Spannung von 220 Volt aus der Netzspannung erzeugt.
| 4-5. Funktion des Mikrowellenherdes | zum Seitenanfang  |
Anders als beim Kochen, wo das Essen von außen nach innen erwärmt wird, dringen bei einer Mikrowelle die Strahlen schnell ins Innere des Garguts ein (die Strahlen werden absorbiert). Dabei werden die Nahrungsbestandteile in extreme Rotation versetzt.
| 4-6. Wirkungsgrad | zum Seitenanfang  |
Ein Elektroherd setzt beinah 100% der elektrischen Energie in Wärmeenergie um, wobei eine Mikrowelle nur 60 bis 80% der elektrischen Energie in Mikrowellenstrahlung umsetzt; die übrige Energie wird zu Abwärme. Bei kleineren Portionen, etwa 250 ml Flüssigkeit oder 250g einer wasserhaltigen Substanz, ist es energetisch günstiger die Mikrowelle zu verwenden, ansonsten ist der Elektroherd besser.
| 4-7. Weitere Anwendungsgebiete | zum Seitenanfang  |
Mikrowellenherde werden für Synthesen in analytischen Labors verwendet. Die feste oder flüssige Probe wird eingewogen und zum Beispiel mit Säure aufgeschlossen. Dabei werden anorganische Substanzen vollständig gelöst und organische Substanzen in Mineralien überführt. Die Vorteile dieser Mikrowellensynthesen sind, dass man kürzere Reaktionszeiten und höhere Ausbeuten erzielt. Weiterhin werden sie als Alternative zu Autoklaven zur Herstellung von Faserverbundwerkstoffen eingesetzt. Hierbei ist die enorme Energieersparnis von Bedeutung, da nur das Werkstück erhitzt wird.
Ein weiterer Einsatz ist das Trocknen verschiedener Materialien.
| 5. Chemie mit Mikrowelle im Fehling-Lab | zum Seitenanfang  |
| 5-1. Was ist das Fehling Lab? | zum Seitenanfang  |
Im Fehling Lab wird Kindern und Jugendlichen sowie ihren Lehrern die Möglichkeit gegeben, selbstständig zu experimentieren. Das Ziel dabei ist, das Interesse an Naturwissenschaften zu wecken und so auch das Bedürfnis nach wissenschaftlichen Berufen hervorzurufen.
In der ersten Phase soll die Neugier von Kindern der Klassen 3 und 4 gegenüber Naturwissenschaften geweckt und gefördert werden. Gleichzeitig werden dadurch den Lehrern Anregungen für Experimente in ihrem eigenen Schulunterricht gegeben.
Die Besonderheit am Fehling Lab ist, dass das Interesse und die Neugier durch Produkte aus dem Alltag geweckt werden. Die einfachen, altersgemäßen und motivierenden Versuche reizen die Kinder zum Nachmachen oder Weitermachen an. Die Lehrer*innen werden aktiv mit eingebunden, da sie selber mit experimentieren und so angeregt werden, vergleichbare Themen in ihrem Unterricht aufzugreifen. Die Kinder erhalten auch die richtige Ausrüstung wie Laborbrille, Labormantel und die Geräte. Dadurch wird ein emotionaler Bezug geschafft, sodass sich die Kinder als "kleine Chemiker" fühlen.
Das Fehling Lab hält auch Fortbildungen für Lehrer*innen und bildet Lehramtsstudenten aus.
| 5-2. Vorwort | zum Seitenanfang  |
Ich habe alle Versuche des Stuttgarter Fehling Labs mehrere Male getestet und konnte so einige optimieren. Jedoch ist es mir nicht gelungen, alle Versuche zu optimieren, da es bereits meiner Meinung nach die bestens Angaben waren.
Zuerst werden die Versuche mit der jeweiligen Beobachtung und mit verschiedenen Einwaagen, Zeiten, Zusammensetzungen unter anderem genannt und anschließend die fertigen, optimierten Versuchsdurchführungen.
| 5-3. Die Versuche | zum Seitenanfang  |
| 5.3.1. Versuche im Fehling-Lab |
| 1. Popcorn-Versuch | |||||||||
|
|||||||||
| 2. Luftballon-Versuch: | |||||||||
|
Durch einige Versuche fand man heraus, dass bei 800 Watt und 1mL vorgelegtem Wasser etwa 25 Sekunden benötigt werden bis sich der Ballon aufbläst. Bei 5mL vergehen etwa 15 Sekunden und bei 10mL weniger als 10 Sekunden. Jedoch bläst sich bei 10mL Wasser der Ballon so schnell auf, dass man befürchten muss, er würde in der Mikrowelle platzen. Weiterhin sollten farbige Ballons verwendet werden, da dunkle Ballons in der Mikrowelle kaum sichtbar sind. Wird weniger Watt verwendet, benötigt der Luftballon mehr Zeit sich aufzublasen.
|
|||||||||
| 3. Hot- Spot- Ermittlung: | |||||||||
|
Der Hot- Spot wurde mehrmals laut Versuchsdurchführung ermittelt. |
|||||||||
| 4. Kunststoffe in der Mikrowelle: | |||||||||
|
Es wurden Kunststoffgegenstände aus dem täglichen Bedarf für 1-2 Minuten in die Mikrowelle gestellt und beobachtet. Unter anderem Einwegtrinkbecher, Puddingbecher, Fruchtzwergbecher, Jogurtbecher, Einwegbesteck, Plastikverpackungen und Verpackungen von Fertiggerichten. Keiner der angegebenen Kunststoffe veränderte sich nach 1 Minute. Alle behielten ihre Form bei und schmolzen nicht. Die Kunststoffproben von der Arbeitsgemeinschaft Deutsche Kunststoff Industrie AKI wurden im Fehling Lab in der Universität Vaihingen von mir getestet. Nur das Polyamid begann nach kurzer Zeit zu schmelzen. |
|||||||||
| 5. Citronensäure und Glycerin: | |||||||||
|
Um diesen Versuch zu optimieren, änderte ich die Zusammensetzung von Glycerin und Citronensäure. Die Höhe von 800 Watt behielt ich bei, da bei niedriger Wattzahl das Ergebnis unzureichend war.
|
|||||||||
| 6. Wassergehalt verschiedener Fette: | |||||||||
|
Bei diesem Versuch könnte ich keine Optimierung erzielen. Ich habe nur festgestellt, dass die Halbfettbutter am schnellsten schmilzt und das Frittierfett am längsten Zeit benötigt. Daher wird die Versuchsdurchführung des Fehling Labs übernommen. |
|||||||||
| 7. Erwärmen eines Zwei- Phasen- Systems: | |||||||||
|
|||||||||
| 8. Zucker-Stärke-Vergleich: | |||||||||
|
Es konnte hierbei keine Optimierung erzielt werden. Es konnte nur das Ergebnis festgestellt werden, dass nach etwa 3 Minuten der Traubenzucker auskaramellisierte, während sich der Zucker und die Stärke noch nicht verändert hatten. |
|||||||||
| 9. Entwässern von Kupfersulfat-Pentahydrat (Kupfervitriol): | |||||||||
|
Bei diesem Versuch konnte nichts optimieret werden. Ich habe einige Male Kupfersulfat-Pentahydrat entwässert, um zu schauen, nach welcher Zeit es fast komplett entwässert ist. Auf diese Weise konnte bei allen Versuchen mehr als 90% des Wassers abgetrennt werden. Dies ist auch durch die Entfärbung des Kupfervitriols sichtbar. Es geht von leuchtend blau nach weiß-hellblau über. Das 100%ige Entwässern des Kupervitriols konnte nicht erreicht werden. |
|||||||||
| 10. CD-Versuch | |||||||||
| Der CD-Versuch wurde gemäß Versuchsdurchführung mehrmals getestet. Da es innerhalb weniger Sekunden bereits zur Funkenbildung kommt und die CD "innerlich zerspringt" konnte nichts optimiert werden. | |||||||||
| 11. Aktivkohle | |||||||||
| Den Aktivkohle-Versuch habe ich mehrmals ausprobiert. Dabei ist mir aufgefallen, dass mit Aktivkohle ein Plasma hergestellt werden kann. Erläuterungen dazu folgen später (siehe Plasmaerzeugung 5.4.15.). | |||||||||
| 5.3.2. Versuche außerhalb des Fehling-Labs |
| 1. Entwässern von Nickelsulfat-Hexahydrat und Cobaltsulfat-Heptahydrat | |||
| Nickelsulfat-Hexahydrat und Cobaltsulfat-Heptahydrat lassen sich ähnlich gut entwässern wie Kupfersulfat-Pentahydrat. Es werden auch über 90% des enthaltenden Wassers abgeschieden. In beiden Fällen ist eine Entfärbung sichtbar. Da jedoch Nickel- und Cobaltsalze aufgrund ihrer Giftigkeit für das Fehling Lab nicht geeignet sind, wurde der Versuch dann abgebrochen. Die Versuchsdurchführungen entsprechen der von Kupfervitriol und werden nicht mehr gesondert aufgeführt. | |||
| 2. Entwässern von Calciumsulfat-Dihydrat: | |||
|
Durch mehrere Versuche konnte ich feststellen, dass Calciumsulfat-Dihydrat bis zu Calciumsulfat mit einem halben Kristallwasser entwässert werden konnte. Bis dorthin benötigt es circa 15 Minuten. Eine vollständige Entwässerung konnte ich nicht erreichen. Die Versuchsdurchführung entspricht der von Kupfervitriol und wird nicht mehr gesondert aufgeführt. Ein Auswertungsbeispiel:
|
|||
| 3. Synthese von Phenolphthalein und Fluoreszein in der Mikrowelle | |||
|
|||
| 4. Luft-Wasser-Wasser (mit Alufolie abgeschirmt)-Salzwasser-Öl | |||
| Der Versuch wurde laut Versuchsdurchführung mehrere Male getestet. Es lassen sich die gleichen Ergebnisse beobachten, aber keine Optimierung erzielen. | |||
| 5. Plasmaerzeugung | |||
|
|||
| 6. Playmobil | |||
| Es wurde ein Playmobilmännchen für 4 Minuten in die Mikrowelle gestellt. Nach einer Minute sind ein Teil des Armes und ein Teil des Beines geschmolzen. Nach einer weiteren Minute löste sich bereits der untere Teil vom oberen Teil. Und schließlich nach fast 4 Minuten war das Männchen so weit geschmolzen, dass man den Rumpf vom Kopf trennen konnte. | |||
| 7. Cremeherstellung | |||
|
Die Creme wurde mit den in der Versuchsdurchführung angegebenen Chemikalien in der Mikrowelle hergestellt. Bereits beim ersten Versuch ließ sich eine hervorragend geschmeidige Creme herstellen. Als Duft verwendete ich verschiedene Parfumöle der Firma "CAELO". Diese waren: Parfümöl Grüner Apfel Durch Fragen und Testen der Creme mehrerer Mitschüler und Assistenten kam als Ergebnis heraus, dass die Creme schnell einzieht, schön geschmeidig ist, der Haut Feuchtigkeit liefert und das Vanille-Aroma am beliebtesten ist. |
|||
| 8. Herstellen eines Polyesters aus Citronensäure und Rizinusöl | |||
|
Es wurde aus Citronensäure und Rizinusöl ein Ester hergestellt. Bei ihm ließen sich, im Gegensatz zu dem Ester aus Citronensäure und Glycerin, keine gute Fäden ziehen, da ein bernsteinfarbenes Harz entsteht. Der Nachteil dieses Esters ist, dass er schlecht wasserlöslich ist; daher sollten die verwendeten Gefäße rasch gereinigt werden. Weiterhin entwickelt Rizinusöl beim Erhitzen einen unangenehmen Geruch. Daher ist dieser Versuch fürs Fehling Lab weniger geeignet.
|
|||
| 5-4. Versuchsdurchführungen | zum Seitenanfang  |
| 5.4.1. Popcorn-Versuch |
| Geräte- und Materialbedarf: | Eine Mikrowelle, ein 250mL Becherglas, ein passendes Uhrglas und Maiskörner |
| Vorbereitung: | Einige Maiskörner in das Becherglas geben und mit dem Uhrglas abdecken. Die Mikrowelle auf 800 Watt stellen. |
| Versuchsdurchführung: | Das mit den Maiskörnern gefüllte Becherglas in die Mikrowelle auf die Mitte des Drehtellers stellen. Die Zeitschaltuhr auf etwa 2 Minuten einstellen. |
| Beobachtung: | Nach etwa 1 Minute platzen die Maiskörner auf und Popcorn entsteht. |
| Erklärung: | Die Maiskörner enthalten in ihrem Inneren viel Feuchtigkeit. Durch die Mikrowellenstrahlen wird diese Feuchtigkeit im Inneren schneller erwärmt als die Schale. Durch das verdampfende Wasser entsteht im Korn ein Überdruck, sodass das Maiskorn aufplatzt. |
| 5.4.2. Luftballon-Versuch |
| Geräte- und Materialbedarf: | Eine Mikrowelle, zwei farbige Luftballone und eine 10mL Pipette |
| Vorbereitung: | Den ersten Luftballon ohne Wasser mit einem Knoten verschließen. In den zweiten mit Hilfe der Pipette 5mL Wasser einfüllen und ebenfalls verschließen. Die Mikrowelle auf 800 Watt einstellen. |
| Versuchsdurchführung: | Beide verschlossenen Luftballone in die Mikrowelle legen und die Zeitschaltuhr auf 1 Minute stellen. |
| Beobachtung: | Der mit Wasser gefüllte Luftballon bläst sich nach wenigen Sekunden auf. Nach dem Öffnen der Mikrowellentür kühlt der Luftballon ab und fällt wieder in sich zusammen. Der leere Ballon zeigt keine Veränderung. |
| Erklärung: | In dem leeren Luftballon befindet sich nur Luft, die sich nicht anregen lässt. Hingegen das Wasser lässt sich anregen. Es erwärmt sich dabei, sodass Wasserdampf entsteht, der den Ballon aufbläst. Beim Abkühlen kondensiert der Dampf wieder, wird zu Wasser und der Ballon fällt zusammen. |
| 5.4.3. Hot-Spot-Ermittlung |
| Geräte- und Materialbedarf: | Eine Mikrowelle, zugeschnittene Kunststoffplatte (Styroporplatte auch geeignet), Thermo-Fax-Papier, Küchenkrepp, Wasserzerstäuber, Klebestreifen (Tesa-Film), Filzstift |
| Vorbereitung: | Fax-Papier auf die Größe der Kunststoffplatte zuschneiden. Die Kunststoffplatte mit Küchenkrepp belegen und mit dem Wasserzerstäuber gut anfeuchten. Anschließend mit dem zugeschnittenen Thermo-Fax-Papier abdecken (Oberseite nach oben, bei Nagelprobe erkennbar durch Schwärzung) und dieses mit Klebestreifen befestigen. Den Glasteller und den Träger entfernen. Die bezogene Kunststoffplatte einsetzen. Die Mikrowelle auf 800 Watt einstellen. |
| Versuchsdurchführung: | Auf der Zeitschaltuhr 1 Minute einstellen und starten. Wenn der Hot-Spot schon vor Ablauf der Zeit gut sichtbar ist, die Mikrowelle stoppen. Die Hot-Spot-Stelle mit einem Stift kennzeichnen. Den Träger und den Glasteller wieder einsetzen. |
| Beobachtung: | Ohne Drehteller ergeben sich für jede Mikrowelle typische schwarze Bereiche, die sogenannten Hot-Spot-Zonen. |
| Erklärung: | Im Ofenraum kommt es durch Reflexion der Mikrowellen an den Innenwänden zu Interferenzen, was zu einem inhomogenen elektromagnetischen Feld führt. Mikrowellenfelder von Haushaltsmikrowellen zeigen Bereiche vollständiger Feldlöschung einerseits und andererseits so genannter Hot-Spots; das sind Bereiche erhöhter Strahlungsintensität. Das Problem wird technisch durch den Einbau des Glasdrehtellers gelöst, auf dem das zu erhitzende Gut kontinuierlich durch die Löschungszonen und die Hot-Spots bewegt und so homogen erhitzt wird. In den Hot-Spot-Zonen des inhomogenen Mikrowellenfelds erhitzt sich das feuchte Thermofaxpapier sehr viel schneller und das Wasser verdampft hier früher als in den übrigen Flächenbereichen des Papiers. Der heiße Wasserdampf verursacht die Schwärzung des Thermopapiers. |
| 5.4.4. Kunststoffe in der Mikrowelle |
| Geräte- und Materialbedarf: | Eine Mikrowelle, Kunststoffgegenstände aus dem täglichen Bedarf (Jogurtbecher, Trinkbecher, Kunststoffgeschirr, Kunststoffpipette), Kunststoffproben von der Arbeitsgemeinschaft Deutsche Kunststoff Industrie AKI: Polystyrol PS, Polypropylen PP, Polyvinylchlorid PVC, Polyethylen PE, Polyamid PA, Papier, Probenblatt für Kunststoffproben |
| Vorbereitung: | Die Mikrowelle auf 800 Watt einstellen. |
| Versuchsdurchführung: | Die verschiedenen Haushaltsgegenstände aus Kunststoff auf einem Blatt Papier kreisförmig auf dem Drehteller der Mikrowelle anordnen. Die Proben in der Mikrowelle 2 Minuten erhitzen. In einem zweiten Durchgang Kunststoffproben auf das vorbereitete Probenblatt geben und ebenso verfahren. |
| Beobachtung: | Die Kunststoffgegenstände des alltäglichen Bedarfs verändern sich nach 1 Minute und 800 Watt nicht. Von den Kunststoffproben verändert sich unter diesen Bedingungen nur das Polyamid. |
| Erklärung: | Die unpolaren Kunststoffmoleküle PS, PP, PVC und PE werden in der Mikrowelle nicht angeregt. Das Molekül von PA besitzt C=O-Doppelbindungen und NH-Gruppen, ist polar, kann Wasserstoffbrücken ausbilden und verändert daher bei diesen Bedingungen bereits seine Eigenschaften. |
| 5.4.5. Citronensäure und Glycerin |
| Geräte- und Materialbedarf: | Eine Mikrowelle, Ein Becherglas (100mL), Ein Uhrglas, Citronensäure, Glycerol (85%), eine Laborwaage |
| Vorbereitung: | 7 g Citronensäure und 1,5-1,7 g Glycerol in ein Becherglas einwiegen und die Mikrowelle auf 800 Watt stellen. |
| Versuchsdurchführung: | Das Becherglas an den Rand der Mikrowelle stellen. Die Mikrowelle auf 1 Minute stellen und starten. Sobald die Citronensäure vollständig gelöst ist, wird die Flüssigkeit auf ein Uhrglas gegossen. |
| Beobachtung: | Die Citronensäure löst sich in dem Glycerol vollständig auf. Das Wasser verdampft und die Lösung siedet. Nachdem sich die Lösung auf dem Uhrglas abgekühlt hat, können sich mit einem Draht oder einem Spatel Fäden ziehen lassen. Diese lassen sich aufwickeln. Die Lösung darf nicht zu lange erhitzt werden, da sonst unangenehm riechende Substanzen entstehen, die sich braun verfärben. |
| Erklärung: | Es entsteht aus der Citronensäure und dem Glycerol ein Polyester. Es handelt sich hierbei um eine Polykondensation, da Wasser abgespalten wird. Im noch flüssigen Zustand lassen sich Endlosfäden ziehen, da der Polyester sehr elastisch ist. Nach dem Abkühlen wird die Lösung zu einer harten Masse, mit der sich beispielsweise Glasplatten verbinden lassen. Dieser Polyester ist wasserlöslich, sodass sich die Geräte problemlos reinigen lassen. |
| 5.4.6. Wassergehalt verschiedener Fette |
| Geräte- und Materialbedarf: | Eine Mikrowelle, drei Reagenzgläser, ein Becherglas (100mL), ein Spatel, Butter, Halbfettbutter, Frittierfett (Butterschmalz), etwas Watte, Stoppuhr und ein Filzstift. |
| Vorbereitung: | Es wird von jedem Fett eine Spatelspitze in 1 Reagenzglas gegeben und das Reagenzglas mit Filzstift beschriftet. Das Reagenzglas wird mit Watte verschlossen, um Fettspritzer zu verhindern. Die Mikrowelle auf 360 Watt stellen. |
| Versuchsdurchführung: | Es werden nacheinander die Reagenzgläser in ein Becherglas an den Rand des Drehtellers gestellt. Die Position sollte bei allen Proben immer dieselbe sein, um einen Vergleich anstellen zu können. Mit Hilfe der Stoppuhr wird die Zeit bis zum vollständigen Schmelzen festgehalten. |
| Beobachtung: | Das Frittierfett schmilzt als letztes und die Halbfettbutter benötigt am wenigsten Zeit. |
| Erklärung: | Die unpolaren Fettmoleküle werden kaum angeregt. Umso mehr werden die polaren Wassermoleküle in dem Fett angeregt, weshalb es auch zur Erwärmung kommt. Das bedeutet, je mehr Wasser ein Fett enthält, desto schneller schmilzt es. Somit enthält Halbfettbutter das meiste Wasser und Frittierfett am wenigsten Wasser. |
| 5.4.7. Erwärmen eines Zwei-Phasen-Systems |
| Geräte- und Materialbedarf: | Eine Mikrowelle, drei Bechergläser (250mL), zwei Uhrgläser, eine Heizplatte (oder ein Brenner mit Dreifuß und Drahtnetz), ein kleiner Messlöffel, eine 25mL Pipette, Siedesteine, Schutzhandschuhe, Schutzbrille, Haushaltszucker, Methylenblau oder Tinte. |
| Vorbereitung: | In einem 250mL Becherglas werden 10 Messlöffel Zucker in 50mL Wasser gelöst und einige Tropfen Methylenblau zugegeben. In den beiden restlichen Bechergläsern werden 100mL Wasser vorgelegt und 2 Siedesteine zugefügt. Das Wasser mit 25mL der angefärbten Zuckerlösung nun langsam unterschichten. Dies funktioniert gut, indem man die Spitze der Pipette auf den Boden des Becherglases setzt und die Zuckerlösung langsam auslaufen lässt. Die Bechergläser mit den Uhrgläsern abdecken. Die Mikrowelle auf 800 Watt und die Heizplatte auf höchste Stufe einstellen bzw. den Brenner aufstellen und anzünden. |
| Versuchsdurchführung: | Das erste Becherglas wird an den Rand des Drehtellers in die Mikrowelle gestellt und die Zeitschaltuhr auf 1 Minute eingestellt. Nach Erreichen des Siedepunktes wird das Becherglas vorsichtig aus der Mikrowelle genommen. Das zweite Becherglas wird auf die Heizplatte gestellt, zum Sieden erhitzt und anschließend heruntergenommen. |
| Beobachtung: | Auf der Heizplatte durchmischen sich die zwei Phasen bereits vor Erreichen des Siedepunktes. In der Mikrowelle durchmischen sich die Phasen nicht so schnell. Sie bleiben selbst beim Sieden noch längere Zeit erhalten. Weiterhin beginnt in der Mikrowelle die Lösung sehr viel schneller zu sieden. |
| Erklärung: | In der Mikrowelle wird das Wasser gleichmäßiger erhitzt. Dadurch tritt das Sieden früher auf und ist im Vergleich zum Sieden auf der Heizplatte ruhiger. Die Phasen bleiben trotz Erreichen des Siedepunktes erhalten; man sieht nur einige Gasblasen an der Becherglaswand empor steigen. Die Polarität der Substanz ist verantwortlich für eine gleichmäßige Erwärmung in der Mikrowelle. Auf der Heizplatte bzw. auf dem Brenner wird das Wasser viel ungleichmäßiger erhitzt. Aufgrund der Wärmekonvektion und der damit verbundenen aufsteigenden Gasblasen vermischen sich die zwei Phasen bereits vor dem Sieden. |
| 5.4.8. Zucker-Stärke-Vergleich |
| Geräte- und Materialbedarf: | Eine Mikrowelle, drei Petrischalen, ein Spatel, Haushaltszucker (Saccharose), Traubenzucker (Dextrose/Glucose), Speisestärke |
| Vorbereitung: | Von jedem Produkt eine Spatelspitze in je eine Petrischale geben. Die Mikrowelle auf 800 Watt einstellen. |
| Versuchsdurchführung: | Alle drei Petrischalen in gleichmäßigem Abstand zur Mitte auf dem Glasdrehteller anordnen. Die Zeitschalltuhr auf 5 Minuten einstellen. |
| Beobachtung: | Nach ca. 4 Minuten beginnt die Dextrose zu karamellisieren, die Saccharose und die Speisestärke verändern sich nach dieser Zeit noch nicht. |
| Erklärung: | Die Dextrose verändert sich bei diesen Bedingungen, da das enthaltene Kristallwasser die Wärmeenergie schneller aufnimmt. Der Haushaltszucker würde bei weiterer Energiezufuhr ebenfalls karamellisieren und die Stärke "verkohlen". |
| 5.4.9. Entwässern von Kupfersulfat-Pentahydrat (Kupfervitriol) |
| Geräte- und Materialbedarf: | Eine Mikrowelle, ein Becherglas (250mL), eine Analysenwaage, ein Spatel, Schutzhandschuhe, ein Rundfilter, Kupfersulfat-Pentahydrat |
| Vorbereitung: | Zunächst wird das Leergewicht des Becherglases auf der Analysenwaage ermittelt. Anschließend wird eine genaue Menge von ungefähr 250mg Kupfervitriol eingewogen. Mikrowelle auf 800 Watt einstellen und die Zeitschaltuhr auf 3 Minuten stellen. |
| Versuchsdurchführung: | Das Becherglas wird in die Mitte des Drehtellers in die Mikrowelle gestellt und mit einem Rundfilter abgedeckt. Das Kupfersulfat-Pentahydrat wird 3 Minuten erhitzt, aus der Mikrowelle genommen und nach kurzem Abkühlen gewogen. Dieser Vorgang wird so lange wiederholt, bis man ein konstantes Gewicht erhält. Anschließend ist mit unten stehender Berechnung der theoretische Wert zu ermitteln. |
| Beobachtung: | Es ist eine Entfärbung des Kupfervitriols zu sehen. |
| Erklärung: | Durch die zugeführte Energie wird das Kristallwasser angeregt und spaltet sich dadurch ab. |
| Quantitative Auswertung: | x=theoretischer Wert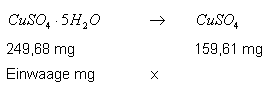 |
| 5.4.10. CD-Versuch |
| Geräte- und Materialbedarf: | Eine Mikrowelle, eine alte CD, ein Blatt Papier oder Küchenkrepp. |
| Vorbereitung: | Die Mikrowelle auf 90 Watt stellen. Das Papier/Küchenkrepp auf den Glasteller legen. |
| Versuchsdurchführung: | Die CD wird mir der Spurenseite nach oben auf den mit dem Papier abgedeckten Glasdrehteller in die Mikrowelle gelegt und mit der Zeitschaltuhr (max. 0,5 Minuten einstellen) gestartet. |
| Beobachtung: | Nach wenigen Sekunden kommt es zur Funkenbildung. |
| Erklärung: | Die aufgedampfte Metallschicht verhält sich wie eine Antenne. Die Energie wird aufgenommen und in kinetische Energie der frei beweglichen Elektronen des Metalls umgewandelt. Genau betrachtet, befinden sich die Elektronen in einem elektrischen Feld, in dem sie von Minus nach Plus beschleunigt werden. Dieses elektrische Feld wechselt in einem Mikrowellenofen knapp zweieinhalbmilliardenmal pro Sekunde. Das führt dazu, dass die Elektronen extrem schnell hin- und herbeschleunigt werden. Dabei nehmen sie teilweise so viel Energie auf, dass sie (vereinfacht gesagt) kurzfristig in höhere Elektronenbahnen wechseln und beim Verlassen dieser Bahnen helle Lichtimpulse aussenden. Zudem erhitzt die Elektronenbewegung die Metallschicht an einigen Stellen so stark, dass sie zu glühen beginnt und verdampft. Genau an diesen Stellen entstehen die Risse, durch die man hindurchsehen kann. |
| 5.4.11. Aktivkohle |
| Geräte- und Materialbedarf: | Eine Mikrowelle, ein Reagenzglas, ein Becherglas, Aktivkohle gekörnt |
| Vorbereitung: | Das Reagenzglas etwa 1 cm hoch mit der Aktivkohle füllen. Das Reagenzglas in ein kleines Becherglas stellen. Die Mikrowelle auf 800 Watt stellen. |
| Versuchsdurchführung: | Das Becherglas auf den Glasdrehteller in die Mikrowelle stellen (nicht in die Mitte) und mit der Zeitschaltuhr starten. Nach 30 Sekunden abschalten. |
| Beobachtung: | Nach wenigen Sekunden kommt es zur Funkenbildung an der Aktivkohle. |
| Erklärung: | Aktivkohle lässt sich von der Mikrowellenstrahlung anregen, erklären lässt sich das durch das teilweise delokalisierte Elektronensystem und den hohen elektrischen Innenwiderstand aufgrund der ausgeprägten Porenstruktur. Die dabei erzeugten hohen Temperaturen nützt man in der Graphit-Suszeptor-Tiegel-Technik bei der Glasherstellung aus. Ausgangspunkt ist die gute Suszeptibilität des graphitischen Kohlenstoffs. |
| 5.4.12. Synthese von Phenolphthalein |
| Geräte- und Materialbedarf: | Eine Mikrowelle, ein Becherglas (100mL), ein Spatel, eine Laborwaage, eine 10mL Messpipette |
| Chemikalien: | Phthalsäureanhydrid: 1g Phenol: 1g Schwefelsäure (96%): 2 Tropfen Ethanol: 1mL |
| Versuchsdurchführung: | Phthalsäureanhydrid, Phenol und Schwefelsäure werden auf der Laborwaage in ein Becherglas eingewogen und gemischt. Die Mikrowelle wird auf 360 Watt und auf 1 Minute eingestellt. Die Mikrowelle wird gestartet. Sollte nach dieser Zeit noch keine Schmelze vorliegen, erneut auf 1 Minute stellen. Die Schmelze wird noch eine weitere Minute bei einer Temperatur von etwa 120°C in der Mikrowelle gehalten. |
| Beobachtung: | Eine klare Lösung mit leichtem Violettstich wird erhalten. |
| Aufarbeitung: | Die Schmelze wird kurz abgekühlt und mit ca. 1mL Ethanol extrahiert. Der Extrakt lässt sich als Indikatorlösung verwenden. |
| 5.4.13. Synthese von Fluoreszein |
| Geräte- und Materialbedarf: | Eine Mikrowelle, ein Becherglas (100mL), ein Becherglas (250mL),ein Spatel, eine Laborwaage, 10mL Messpipette |
| Chemikalien: | Phthalsäureanhydrid: 0,1g Resorcin: 0,1g Zinkchlorid: 0,2g Verd. Natronlauge: 10mL |
| Versuchsdurchführung: | Phthalsäureanhydrid, Resorcin und Zinkchlorid werden in das 100mL Becherglas gegeben und gemischt. Das Becherglas wird in die Mikrowelle bei 360 Watt gegeben und erhitzt bis eine Schmelze entstanden ist. Die Schmelze wird noch kurz in der Mikrowelle gehalten und anschließend abgekühlt. Die noch flüssige Mischung in ein Becherglas mit ca. 200mL Wasser, das mit 10mL verdünnter Natronlauge alkalisch gemacht wurde, einfließen lassen. Sollte keine flüssige Schmelze vorliegen, wird etwas Wasser hinzugegeben und dann in die Wasser-Natronlauge-Mischung gegossen. |
| Beobachtung: | Eine intensiv gelb-grün fluoreszierende Lösung wird erhalten |
| 5.4.14. Luft-Wasser-Wasser(mit Alufolie abgeschirmt )-Salzwasser-Öl |
| Geräte- und Materialbedarf: | Eine Mikrowelle, 5 kleine Schnappdeckelgläser (20-30mL), Wasser, Kochsalz, Öl, Aluminiumfolie |
| Vorbereitung: | 3 Schnappdeckelgläser werden gleich hoch mit Wasser gefüllt. Eins davon wird mit Aluminiumfolie umwickelt und in dem zweiten wird eine Spatelspitze Kochsalz gelöst. Das vierte Schnappdeckelglas wird gleich hoch mit Öl (Speiseöl oder Paraffinöl) gefüllt. Die vier gefüllten Schnappdeckelgläser werden verschlossen und das fünfte wird nur mit Luft gefüllt verschlossen. Die Gläser werden noch entsprechend beschriftet. |
| Versuchsdurchführung: | Die Schnappdeckelgläser werden nacheinander 20 Sekunden bei 800 Watt in die Mikrowelle gegeben und anschließend mit der Hand oder einem digitalen Thermometer die Temperatur gemessen und verglichen. |
| Beobachtung: | Das mit Öl, mit Luft und mit Aluminiumfolie umgebene Schnappdeckelglas erwärmt sich kaum. Wasser erwärmt sich. Mit Kochsalz erwärmt es sich noch stärker. |
| Erklärung: | Luft kann nicht angeregt werden und wird somit nicht erwärmt. Ebenso wird das unpolare Öl nur wenig angeregt und kaum erwärmt. Die Aluminiumfolie schirmt die Mikrowellenstrahlung ab, d.h. Mikrowellenstrahlen können nicht durch die Folie, um das Wasser zu erwärmen. Das polare Wasser wird durch die Strahlung angeregt und erwärmt sich dadurch. Eine hingegen stärkere Erwärmung zeigen die Salz-Ionen im Wasser durch eine stärkere Anregung der Mikrowellenstrahlen. |
| 5.4.15. Plasmaerzeugung |
Hinweise bei der Plasmaerzeugung:
Man nimmt ein Teller aus Ton oder Keramik, um zu verhindern, dass der Glasdrehteller aufgrund der enormen Hitze beschädigt wird.
Wenn das Plasma ganz kurz beobachtet wurde, muss die Mikrowelle sofort ausgeschaltet werden. Eine Plasmaerzeugung ist nicht ganz ungefährlich und es kann zu Zerstörung der Gefäße kommen oder Schlimmeres passieren. Daher die Mikrowelle nur ganz kurz anlassen.
Die Gefäße sind danach sehr heiß. Also Schutzhandschuhe und eine Schutzbrille bei allen vier Versuchen verwenden.
| 5.4.15.1. Plasma mit Aktivkohle |
| Geräte- und Materialbedarf: | Eine Mikrowelle, Aktivkohle gekörnt, ein Reagenzglas, ein kleines Becherglas, ein Teller aus Keramik oder Ton, Schutzhandschuhe, Schutzbrille |
| Vorbereitung: | Das Reagenzglas etwa 1 cm hoch mit der Aktivkohle füllen. Das Reagenzglas in ein kleines Becherglas stellen. Die Mikrowelle auf 800 Watt stellen. |
| Versuchsdurchführung: | Den Teller in die Mikrowelle legen und das Becherglas darauf stellen (nicht in die Mitte) und mit der Zeitschaltuhr starten. Nach maximal 40 Sekunden abschalten. |
| Beobachtung: | Zuerst ist eine Funkenbildung sichtbar. Anschließend lässt sich ein leuchtendes Plasma in Form einer hellen Flamme erkennen. |
| Erklärung: | Zusammenfassung siehe: 5.4.15.4 Erklärung |
| 5.4.15.2. Plasma mit Draht |
| Geräte- und Materialbedarf: | Eine Mikrowelle, ein Stück Draht, ein Porzellantiegel, ein Teller aus Keramik oder Ton, Schutzhandschuhe, Schutzbrille |
| Vorbereitung: | Der Draht wird zu einem Kreis gebogen, wobei sich die Enden gegenüberstehen. Die beiden Enden dürfen sich nicht berühren, sodass eine kleine Lücke dazwischen bleibt. |
| Versuchsdurchführung: | Den Draht in den Porzellantiegel stellen. Die Mikrowelle auf 800 Watt und 20 Sekunden einstellen. Den Porzellantiegel in der Mitte des Ton- oder Keramiktellers platzieren. |
| Beobachtung: | Es lässt sich innerhalb weniger Sekunden ein Plasma in der Lücke zwischen den Drahtenden beobachten. |
| Erklärung: | Zusammenfassung siehe: 5.4.15.4. Erklärung |
| 5.4.15.3. Plasma mit einer Traube |
| Geräte- und Materialbedarf: | Eine Mikrowelle, eine Traube, ein Teller aus Keramik oder Ton, Schutzhandschuhe, Schutzbrille |
| Vorbereitung: | Die Traube wird in der Mitte durchgeschnitten. Es muss darauf geachtet werden, dass die Traube nicht komplett halbiert wird. Die Traube muss an den Enden zusammenhängen, sonst kann kein Lichtbogen entstehen. |
| Versuchsdurchführung: | Die Mikrowelle auf 800 Watt und max. 20 Sekunden einstellen. Den Teller in die Mikrowelle legen und die Traube in die Mitte legen. |
| Beobachtung: | Innerhalb weniger Sekunden ist ein deutliches Plasma oberhalb der Traube sichtbar. |
| Erklärung: | Zusammenfassung siehe: 5.4.15.4. Erklärung |
| 5.4.15.4. Plasma mithilfe eines Zahnstochers |
| Geräte- und Materialbedarf: | Eine Mikrowelle, eine Glasschale, ein Zahnstocher (aus Holz), ein Korken, ein Teller aus Ton oder Keramik, Schutzhandschuhe, Schutzbrille |
| Vorbereitung: | Den Teller in die Mikrowelle legen. Den Zahnstocher in den Korken stecken. Die Mikrowelle auf 800 Watt und max. 20 Sekunden einstellen. |
| Versuchsdurchführung: | Den Korken mit dem Zahnstocher nach oben auf den Ton- oder Keramikteller stellen. Den Zahnstocher anzünden und die Glasschale darüber stellen. Türe schließen und die Mikrowelle starten. |
| Beobachtung: | Es erscheint für kurze Zeit ein blauer Blitz; anschließend wird innerhalb der Glasschale das Plasma in Form eines Balles gebildet. Nach etwa 10 Sekunden bleibt ein orangefarbiges Gasgemisch aus O3, NO2, NO3 zurück. |
| Hinweis: | Anschließend sofort lüften. Am Besten den Teller mit der Glasschale im Freien öffnen, dass dort das Gas entweichen kann. |
| Erklärung der Plasmaerzeugung: | Plasma bedeutet "das Formbare". Wird einem Feststoff Energie zugeführt wird er flüssig, bei weiterer Energie wird er gasförmig. Wird nun noch weitere Energie zugeführt, entsteht der sogenannte 4. Aggregatzustand: ein Plasma. Es ist ein Zustand, in dem das Gas ionisiert wird, das heißt die Elektronen werden durch ein Magnetfeld und Hitze von den Atomen gelöst. Die Atome (und Moleküle oder Ionen) und die Elektronen bewegen sich frei umher und wirken gleichzeitig aufeinander. Ein Plasma besitzt andere (besondere) Eigenschaften. |
| 5.4.16. Playmobil |
| Geräte- und Materialbedarf: | Eine Mikrowelle, ein Playmobilmännchen |
| Vorbereitung: | Die Mikrowelle auf 800 Watt und 4 Minuten einstellen. |
| Versuchsdurchführung: | Das Playmobilmännchen wird auf die Mitte des Drehtellers gestellt und die Mikrowelle gestartet. |
| Beobachtung: | Nach bereits 1 Minute lassen sich erste Veränderungen des Männchens beobachten. Nach einigen weiteren Minuten ist das Playmobil teilweise geschmolzen. |
| Erklärung: | Playmobil-Figuren können bis zu ~90% aus Polyamid bestehen. Dieser Kunststoff besitzt C=O-Doppelbindungen und NH-Gruppen. Dadurch, dass Polyamid polar ist, kann er durch Mikrowellenstrahlung angeregt werden und Wasserstoffbrücken ausbilden. Verschiedene Playmobil-Figuren enthalten unterschiedlich viel Polyamid, weshalb die Zeit bis zum Schmelzen variieren kann. |
| 5.4.17. Cremeherstellung |
| Geräte- und Materialbedarf: | Eine Mikrowelle, 2 Bechergläser (150mL), ein Becherglas (250mL), ein Glasstab, ein Spatel und eine Laborwaage |
| Chemikalien: | 25g: Tegomuls 60g: Pflanzenöl (z.B. Sonnenblumenöl, Jojoba) 20g: Konsistenzgeber (z.B. Walratersatz) Parfümöl |
| Versuchsdurchführung: | Alles in ein 250mL Becherglas einwiegen und in der Mikrowelle bei 800 Watt schmelzen. Abkühlen lassen und ab und zu umrühren. 15g der Fettphase in ein 150mL Becherglas einwiegen und in das zweite Becherglas 45g destilliertes Wasser. Das Fett wird erhitzt, bis es geschmolzen ist, und das Wasser wird bis zum Sieden erhitzt. Das heiße Wasser wird zu der flüssigen Fettphase gegeben und solange gerührt, bis es nur noch handwarm ist. Nun noch 8-10 Tropfen des gewünschten Parfümöls zugeben und rühren. Die fertige Creme in eine Cremedose umfüllen. |
| Haltbarkeit: | Die Creme ist mindestens 2 Monate haltbar, aber oft auch länger. |
| 5.4.18. Herstellen eines Polyesters aus Citronensäure und Rizinusöl |
| Geräte- und Materialbedarf: | Eine Mikrowelle, ein Becherglas (150mL), ein Glasstab, ein Spatel und eine Laborwaage |
| Chemikalien: | Citronensäure: 4,5 g Rizinusöl: 10 g |
| Versuchsdurchführung: | Die Citronensäure und das Rizinusöl in das Becherglas einwiegen. Die Mikrowelle auf 800 Watt stellen, Becherglas in die Mitte des Drehtellers stellen und so lange erhitzen, bis sich ein zäher Schaum bildet. Dabei eventuell gelegentlich mit dem Glasstab umrühren. Man lässt abkühlen und erhält ein bernsteinfarbenes, etwas klebriges Harz, das wasserunlöslich ist. |
| Erklärung: | Unter Polykondensation reagieren Citronensäure und Rizinusöl miteinander. Dabei verbinden sich die Hydroxylgruppen des Rizinusöls mit den Carboxylgruppen der Citronensäure zu einem Ester. Gleichzeitig wird durch die Esterbildung Wasser abgespalten. |
| 5-5. Fotos | zum Seitenanfang  |
 |
 |
| Bevor die CD in der Mikrowelle war | Nachdem die CD in der Mikrowelle war |
 |
 |
| Das Playmobilmännchen nach einer Minute in der Mikrowelle | Nach drei Minuten |

Nach vier Minuten in der Mikrowelle

Ein durch die Mikrowellentür fotografiertes Plasma
 |
 |
vor dem Erhitzen in der Mikrowelle (links) und nach dem Erhitzen (rechts). Eine Entfärbung ist sichtbar. |
|
 |
 |
| Eine in der Mikrowelle hergestellte Creme | Ein Polyester aus Citronensäure und Glycerin |
 |
 |
| Ein Polyester-"Faden" | Ein leerer Luftballon (vorne) und ein mit Wasser gefüllter Luftballon (hinten/aufgeblasen) in der Mikrowelle |
| 6. Literaturverzeichnis | zum Seitenanfang  |
Theoretischer Teil:
- http://www.wiley.vch.de/home/phiuz (03.10.07)
- http://www.gdch.de (03.10.07)
- http://www.weltderphysik.de/de/4446.php (03.10.07)
- http://komja.de/?EF&e=14487 (16.01.08)
- http://www.jugendnetz.de/search/showItem.do;jsessionid (16.01.08)
- http://de.wikipedia.org/wiki/Mikrowellenherd (20.12.07)
- http://de.wikipedia.org/wiki/Magnetron (20.12.07)
- http://www.astatine.ch (20.12.07)
Praktischer Teil:
- Skript vom Fehling Lab
- http://www.chemieunterricht.de/dc2/plaste.inhalt1.htm
>> Diese Projektarbeit komplett downloaden / ausdrucken (in PDF)
« zurück zur Übersicht - Projektarbeiten